బెంజీన్
బెంజీన్ ఒక ముఖ్యమైన సేంద్రియ రసాయన సంయోగ పదార్థం. ఇది ఆరోమాటిక్ వర్గానికి చెందిన హైడ్రోకార్బన్. బెంజీన్ యొక్క రసాయన సంకేత పదంC6H6.ఒక అణువు బెంజీన్ లో ఆరు కార్బను, ఆరు హైడ్రోజన్ పరమాణువులు ఆరుభుజాలతోఒక వలయంలా ఏర్పడి ఉండును[11].ముడి పెట్రోలియంలో స్వాభావికంగా ఉండు పదార్థం బెంజీన్. బెంజీన్ అణువులోని కార్బన్ పరమాణువుల మధ్య ఉన్న చక్రీయ అనియత పై బంధం (pi bond) కారణంగా బెంజీన్ను ఆరోమాటిక్ హైడ్రోకార్బన్ గా వర్గీకరించడమైనది.బెంజీన్ రంగులేని, అత్యంత వేగంగా మండుస్వాభావమున్న ద్రవం, ద్రావణి. బెంజీన్ తియ్యని వాసన వెలువరించును.[12] ఇథైల్ బెంజీన్, కుమేన్ (cumene) వంటి సంక్లిష్ట అణునిర్మాణమున్న రసాయన పదార్థాల ఉత్పత్తికి బెంజీన్ ను పూర్వగామిగా (precursor) గా ఉపయోగిస్తారు.బెంజీన్ అధికస్థాయి ఆక్టేన్ సంఖ్య కల్గిఉన్నందున, గాసోలిన్/పెట్రోలు లోని బెంజీన్ అంశీభూతాలలోముఖ్యమైనది.బెంజీన్ క్యాన్సర్ కారణం కనుక పారిశ్రామికేతర వినిమయం పరిమితం
| |||
 Space-filling model
| |||
| పేర్లు | |||
|---|---|---|---|
| IUPAC నామము
Benzene
| |||
| ఇతర పేర్లు
Benzol, Phene, Phenyl hydride
| |||
| గుర్తింపు విషయాలు | |||
| సి.ఎ.ఎస్. సంఖ్య | [71-43-2] | ||
| పబ్ కెమ్ | 241 | ||
| యూరోపియన్ కమిషన్ సంఖ్య | 200-753-7 | ||
| కెగ్ | C01407 | ||
| సి.హెచ్.ఇ.బి.ఐ | CHEBI:16716 | ||
| ఆర్.టి.ఇ.సి.యస్. సంఖ్య | CY1400000 | ||
| SMILES | c1ccccc1 | ||
| |||
| ధర్మములు | |||
| C6H6 | |||
| మోలార్ ద్రవ్యరాశి | 78.11 g·mol−1 | ||
| స్వరూపం | Colorless liquid | ||
| వాసన | Aromatic, gasoline-like | ||
| సాంద్రత | 0.8765(20) g/cm3[1] | ||
| ద్రవీభవన స్థానం | 5.53 °C (41.95 °F; 278.68 K) | ||
| బాష్పీభవన స్థానం | 80.1 °C (176.2 °F; 353.2 K) | ||
| 1.53 g/L (0 °C) 1.81 g/L (9 °C) 1.79 g/L (15 °C)[2][3][4] 1.84 g/L (30 °C) 2.26 g/L (61 °C) 3.94 g/L (100 °C) 21.7 g/kg (200 °C, 6.5 MPa) 17.8 g/kg (200 °C, 40 MPa)[5] | |||
| ద్రావణీయత | Soluble in alcohol, CHCl3, CCl4, diethyl ether, acetone, acetic acid[5] | ||
| ద్రావణీయత in ethanediol | 5.83 g/100 g (20 °C) 6.61 g/100 g (40 °C) 7.61 g/100 g (60 °C)[5] | ||
| ద్రావణీయత in ethanol | 20 °C, solution in water: 1.2 mL/L (20% v/v)[6] | ||
| ద్రావణీయత in acetone | 20 °C, solution in water: 7.69 mL/L (38.46% v/v) 49.4 mL/L (62.5% v/v)[6] | ||
| ద్రావణీయత in diethylene glycol | 52 g/100 g (20 °C)[5] | ||
| log P | 2.13 | ||
| బాష్ప పీడనం | 12.7 kPa (25 °C) 24.4 kPa (40 °C) 181 kPa (100 °C)[7] | ||
| λmax | 255 nm | ||
| అయస్కాంత ససెప్టిబిలిటి | 54.8·10−6 cm3/mol | ||
| వక్రీభవన గుణకం (nD) | 1.5011 (20 °C) 1.4948 (30 °C)[5] | ||
| స్నిగ్ధత | 0.7528 cP (10 °C) 0.6076 cP (25 °C) 0.4965 cP (40 °C) 0.3075 cP (80 °C) | ||
| నిర్మాణం | |||
| Trigonal planar | |||
ద్విధృవ చలనం
|
0 D | ||
| ఉష్ణగతిక రసాయన శాస్త్రము | |||
| నిర్మాణము మారుటకు కావాల్సిన ప్రామాణిక ఎంథ్రఫీ ΔfH |
48.7 kJ/mol | ||
| దహనక్రియకు కావాల్సిన ప్రామాణీక ఎంథ్రఫీ ΔcH |
3267.6 kJ/mol[7] | ||
| ప్రామాణిక మోలార్ ఇంథ్రఫీ S |
173.26 J/mol·K[7] | ||
| విశిష్టోష్ణ సామర్థ్యం, C | 134.8 J/mol·K | ||
| ప్రమాదాలు | |||
| ప్రధానమైన ప్రమాదాలు | potential occupational carcinogen, flammable | ||
| భద్రత సమాచార పత్రము | HMDB | ||
| జి.హెచ్.ఎస్.పటచిత్రాలు |    [8] [8]
| ||
| జి.హెచ్.ఎస్.సంకేత పదం | Danger | ||
| జి.హెచ్.ఎస్.ప్రమాద ప్రకటనలు | H225, H304, H315, H319, H340, H350, H372[8] | ||
| GHS precautionary statements | P201, P210, P301+310, P305+351+338, P308+313, P331[8] | ||
| ఇ.యు.వర్గీకరణ | {{{value}}} | ||
| R-పదబంధాలు | మూస:R45, మూస:R46, R11, మూస:R16, మూస:R36/38,మూస:R48/23/24/25, R65 | ||
| S-పదబంధాలు | S53, S45 | ||
| జ్వలన స్థానం | {{{value}}} | ||
స్వయం జ్వలన
ఉష్ణోగ్రత |
497.78 °C (928.00 °F; 770.93 K) | ||
| విస్ఫోటక పరిమితులు | 1.2–7.8% | ||
| Lethal dose or concentration (LD, LC): | |||
LD50 (median dose)
|
930 mg/kg (rat, oral) | ||
LCLo (lowest published)
|
44,000 ppm (rabbit, 30 min) 44,923 ppm (dog) 52,308 ppm (cat) 20,000 ppm (human, 5 min)[10] | ||
| US health exposure limits (NIOSH): | |||
PEL (Permissible)
|
TWA 1 ppm, ST 5 ppm[9] | ||
REL (Recommended)
|
Ca TWA 0.1 ppm ST 1 ppm[9] | ||
IDLH (Immediate danger)
|
500 ppm[9] | ||
| సంబంధిత సమ్మేళనాలు | |||
సంబంధిత సమ్మేళనాలు
|
Toluene Borazine | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |||
| Infobox references | |||
భౌతిక ధర్మాలు మార్చు
భౌతిక స్థితి మార్చు
బెంజీన్ రంగులేని, పారదర్శకంగా ఉన్నద్రవం. పెట్రోల్ వంటి వాసన కల్గిఉన్నది.బెంజీన్ అణుభారం 78.11184గ్రాములు/మోల్−1.[13]
సాంద్రత మార్చు
బెంజీన్ సాంద్రత 0.8765గ్రాములు/సెం.మీ3
ద్రవీభవన ఉష్ణోగ్రత మార్చు
బెంజీన్ ద్రవీభవన స్థానం 5.53 °C (41.95 °F; 278.68K)
బాష్పీభవన ఉష్ణోగ్రత మార్చు
బెంజీన్ బాష్పీభవన స్థానం 80.1 °C (176.2 °F; 353.2K)
ద్రావణీయత మార్చు
నీటిలో చాలా అల్ప ప్రమాణంలో కరుగును. ఒకలీటరు నీటిలో 0 °C వద్ద 1.53 గ్రాములు, 30 °C వద్ద 1.84 గ్రాములు, 61 °C వద్ద 2.26 గ్రాములు కరుగును.ఇంకా ఆల్కహాల్, కార్బన్ ట్రై క్లోరైడ్ (CHCl3, కార్బన్ టెట్రాక్లోరైడ్ (CCl4, డై ఇథైల్ ఈథర్, ఎసిటోన్, ఎసిటిక్ ఆమ్లంలో కరుగును.
వక్రీభవన గుణకం మార్చు
బెంజీన్ యొక్క వక్రీభవన గుణకం 20 °Cవద్ద: 1.5011, 30°Cవద్ద: 1.4948
స్నిగ్ధత మార్చు
బెంజీన్ యొక్క స్నిగ్ధత 10 °C 0.7528 cP. 40 °C దగ్గర 0.4965cP
చరిత్ర మార్చు
ఐతిహాసికంగా బెంజీన్ అనుపదం, 15 వ శతాబ్ది నుండియు దక్షిణ తూర్పుఆసియా (ఆగ్నేయ ఆసియా) కు చెందిన, 15 వ శతాబ్ది నుండియు యూరోపియన్ మందుల తయారిదార్లకు, సుగంధ ద్రవ్య ఉత్పత్తిదారులకు తెలిసిన గమ్బెంజోయిన్ ( బెంజోయిన్ రెసిన్) నుండి వచ్చింది. బెంజోయిన్ నుండి ఉత్పాదితం ద్వారా అమ్లగుణమున్న రాసాయాన్ని ఉత్పత్తి చేసి, దానికి ఫ్లవర్స్ ఆఫ్ బెంజోయిన్ లేదా బెంజోయిక్ ఆమ్లం అని వ్యవహరించేవారు.ఈ విధంగా బెంజోయిక్ఆమ్లం నుండి ఉత్పతి చేయబడిన ఈ హైడ్రోకార్బన్ కాలక్రమేనా బెంజైన్, బెంజోల్, లేదా బెంజీన్ అని వ్యవహరింపబడింది.
1825లో మొదటగా మైఖేల్ ఫారడే వెలుగించుటకు ఉపయోగించు వాయువు నుండి వేరు చేసి, దీనికి బైకార్బురేట్ ఆఫ్ హైడ్రోజన్ అని నామకరణం చేసాడు.[14] 1833లో ఎయిల్హార్డ్ మిత్స్ చెర్లిష్ (Eilhard Mitscherlich) బెంజోయిక్ ఆమ్లం, సున్నాన్ని కలిపి స్వేదన క్రియద్వారా బెంజీన్ ఉత్పత్తి చేసాడు. ఆయన రసాయన పదార్థాన్ని బెంజైన్ (benzin) అని పిలిచాడు. 1836 లో ఆగస్టు లారెంట్ (Auguste Laurent ) ఈ పదార్థానికి పేరును ఫేనే (phène) గా నిర్ణయించాడు. ఈ పదమే ఇంగ్లీషు పదం ఫెనోల్ ("phenol") కు మూలపదం. ఫెనోల్ అనునది హైడ్రోక్సిలేటేడ్ బెంజీన్. ఫెనైల్ (phenyl", ) అనునది బెంజీన్ నుండి హైడ్రోజన్ పరమాణువు (స్వేచ్ఛా రాడికల్ H•) ను వేరుచేయగా/ సారగ్రహణం చేయగా (abstraction) ఏర్పడిన రాడికల్ పదార్థం. 1845లో ఆగస్టు విలహేం వోన్ హోఫ్ మాన్ (August Wilhelm von Hofmann) తో పనిచేయునపుడు చార్లెస్ మాన్స్ఫీల్డ్ (Charles Mansfield) కోల్ తార్ నుండి బెంజీన్ను వేరు చేసాడు. నాలుగు సంవత్సారాల తరువాత చార్లెస్ మాన్స్ఫీల్డ్ మొదటిసారిగాపారిశ్రామిక స్థాయిలో, కోల్ తార్ విధానంపై ఆధారపడి బెంజీన్ను ఉత్పత్తి చేయడం ప్రారంభించాడు.
మిగతా కెమిస్ట్లు కుడా బెంజీన్కు సంబంధిన రసాయనాలను ఉత్పత్తి కావించడం మొదలుపెట్టారు.1855లో హోఫ్ మాన్ ఆరోమాటిక్అనేపదాన్ని బెంజీన్ కుటుంబానికి చెందిన పదార్థాల సంబంధాన్ని తెలుపుటకు వాడాడు. 1997లో అంతరిక్ష అంతర్భాగంలో బెంజీన్ ఉనికిని గుర్తించారు.
అణు వలయ సౌష్టవం మార్చు
బెంజీన్ రసాయన సంయోగ పదార్థం యొక్క ఎంపిరికల్ ఫార్ములా గురించి చాలా ఏళ్లగాతెలిసి ఉన్నప్పటికీ, అణువులోని ఒక హైడ్రోజన్ పరమాణువు ప్రతి ఒక్కోకార్బన్తో కల్గిఉన్న బహు అసంతృప్త నిర్మాణం (polyunsaturated) చాలాకాలం పెద్ద సవాల్గా ఉండినది. 1858 లో ఆర్చిబాల్డ్ స్కాట్ కోపెర్ (Archibald Scott Couper), 1861లో జోసెఫ్ లోస్చ్మిడస్ట్ (Joseph Loschmidt ) లు పలు ద్విబందాలు కల్గిన పలు వలయాకార అణుసౌష్టవాన్ని ఉహించారు, కాని కెమిస్ట్లకు నిరూపణకు చిన్న ఆధారం/రుజువు లభించలేదు.1865 లో ఫ్రెడ్రిక్ ఆగస్టు కెకులే (Friedrich August Kekulé ) ఫ్రెంచ్ భాషలో ఒక వివరణ/ప్రకటన పత్రాన్ని విడుదల చేసాడు.అందులోఅణువులోని ఆరుకార్బన్లు ఒక ఏకబంధం తరువాత ఒకద్విబంధం, తరువాత ఏకబంధం ఇలా ఒకటి వదలి ఒకటి పద్ధతిలో (alternating ) ఏక, ద్విబందాలు ఏర్పరచు కొనిఉండునని ప్రకటించాడు. మరుసటి సంవత్సరం, జర్మనీ భాషలో ఇంతకన్నా విపులమైన ప్రకటన పత్రాన్ని, ఇదే విషయంపై వివరణపత్రాన్ని విడుదల చేసాడు.
అణునిర్మాణం మార్చు
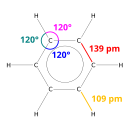
ఎక్సు-కిరణాల వివర్తనం (X-ray diffraction) ద్వారా బెంజీన్ అణువును పరిశీలించగా, కార్బన-కార్బన్లమధ్య దూరం సమానంగా 140 పైకోమీటర్లు (140 pm) ఉంది.ఈ బంధదూర విలువలు, కార్బన్-కార్బన్ల మధ్య ఉండు ద్విబంధ దూరం (135 pm) కన్న ఎక్కువ, ఏకబంధం (147 pm) కన్న తక్కువ.ఈ మధ్యంతర బంధదూర విలువలకు కారణం అణువులలోని పరమాణు ఎలక్ట్రాన్ల స్థానంతరం (delocalization) వలన జరిగింది. కార్బన్-కార్బన్ బంధంలోని ఎలక్ట్రానులు సమానంగా ఆరు కార్బన్ పరమాణువుల మధ్య పంచబడినవి.బెంజీన్ 6 హైడ్రోజన్ పరమాణువుల మాత్రమే కల్గిఉన్నది. ఇది దీని మాతృకలైన ఆల్కేన్, హెక్సేన్ కన్న తక్కువ హైడ్రోజన్ పరమాణువులను కల్గి ఉన్నది
ప్రారంభంలో/మొదట్లో బెంజీన్ వినియోగం మార్చు
19వ శతాబ్ది లో, 20వ శతాబ్ది మొదట్లో బెంజీన్ను, దీనికున్న ఆహ్లాదకరమైన సువాసన కారణంగా ఆప్టర్-షేవ్ లోషన్గా ఉపయోగించేవారు.1920 కి ముందు లోహాల మీది గ్రీజు/కందెన జిడ్డులను తొలగించుటకు పారిశ్రామికద్రావణిగా వినియోగించేవారు.అయితే బెంజీన్ యొక్క విషలక్షణాల గురించి తెలిసిన తరువాత ద్రావణిగా వాడటం మానివేసారు.దీనికి బదులుగా టోలిన్ (toluene ) అనబడు మిథైల్ బెంజీన్ ను ద్రావణిగా ఉపయోగిస్తున్నారు.ఇది బెంజీన్ను పోలిన భౌతికలక్షణాలను కలిగినను, ఇది క్యాన్సరుకారకం కాదు.1903 లో లుడ్విగ్రోసేలియస్ ( Ludwig Roselius) బెంజీన్ ఉపయోగించి కాఫీని డికెఫినేట్ (కేఫిన్ ను కాఫీ, కోకొ గింజలనుండి, తేయాకుఆకుల నుండి తొలగించడం) చెయ్యడం ద్వారా బెంజీన్ వినియాగాన్ని ప్రాచుర్యంలోకి తెచ్చాడు.తరువాతి కాలంలో ఈ విధానానికి స్వస్తి చెప్పారు. ఇతిహాస పరంగా లిగ్విడ్ రెంచ్, పలురంగులను వదలించు/తొలగించు (paint strippers) పదార్థాల తయారి, రబ్బరు సిమెంట్, మచ్చల తొలగించు ఉత్పత్తులలో బెంజీన్ వాడకం గణనీయంగా పెరిగింది. బెంజీన్ ఉపయోగించి చేయుఇలాంటి పదార్థాల ఉత్పత్తి క్రమేనా 1950 నాటికి నిలిచి పోయింది.
లభ్యత మార్చు
అల్ప ప్రమాణంలో బెంజీన్ ను పెట్రోలియం, కోల్/రాకాసి బొగ్గులో గుర్తించారు. పలు పదార్థాలను అసంపూర్ణంగా దహన పరచినపుడు ఉప ఉత్పత్తిగా బెంజీన్ ఏర్పడును. రెండవ ప్రపంచ యుద్ధ సమయం వరకు, ఉక్కుపరిశ్రమకు అవసరమైన కోక్ (coke) ను ఉత్పత్తి చేయునపుడు బెంజీన్ ఉపఉత్పత్తిగా లభ్యమైయ్యేది.టోలిన్.క్సైలెన్ లను ఉత్పత్తి చేయునపుడు బెంజీణ్ విడుదల అగును[15] 1950 నాటికి, పెరిగిన పాలిమర్ పరిశ్రమలకు బెంజీన్ వాడకం పెరిగినందున, బెంజీన్ను పెట్రోలియం నుండి ఉత్పత్తి కావించడం ప్రారంభించారు. వర్తమానకాలంలో అధిక మొత్తంలో బెంజీన్ ఉత్పత్తి పెట్రో కెమికల్ /పెట్రో రసాయన పరిశ్రమలనుండి ఉత్పత్తి చేయబడుచున్నది. అతి తక్కువ ప్రమాణంలో మాత్రం రాకసిబోగ్గు/కోల్ నుండి బెంజీన్ తయారు చేస్తున్నారు.
బెంజీన్ వ్యుత్పన్నములు(derivatives) మార్చు
చాలా ముఖ్యమైన రసాయన సమ్మేళన పదార్థాలు బెంజీన్ నుండి వ్యుత్పన్నముచేయబడుచున్నవి. చాలా ముఖ్యమైన రసాయన సమ్మేళన పదార్థాలు బెంజీన్ నుండి వ్యుత్పన్నముచేయబడుచున్నవి.బెంజీన్ లోని ఒకటి లేదా అంతకన్నా ఎక్కువ హైడ్రోజన్ పరమాణువులను ఇతర ఫంక్షనల్ గ్రూపు (functional group) లతోభర్తీ చెయ్యడం వలన పలు రసాయన సంయోగ పదార్థాల వ్యుత్పన్నము జరుగును. అలా బెంజీన్ నుండి వ్యుత్పన్నం చేసిన రసాయనాలకు ఉదాహరణ ఫేనోల్ (phenol (PhOH) ), టోలిన్ (toluene (PhMe) ), అనిలైన్ (aniline (PhNH2) ). బెంజీన్ రింగులను లింకు చెయ్యడం వలన బైఫెనాయిల్ (biphenyl, C6H5–C6H5) ఏర్పడును. మరింతగా హైడ్రోజన్ పరమాణువు కోల్పోవడం వలన నాప్థాలిన్, అంత్రాసేన్ (anthracene) వంటి కరిగిపోయిన/మిళితమైన (fused) ఆరోమాటిక్ హైడ్రోకార్బన్ లను ఏర్పడును. కొన్ని సందర్భాలలో బెంజీన్ రింగు/వలయం లోని కార్బన్ పరమాణువులను ఇతర మూలకాలతో తొలగించెదరు. చాలా సందర్భాలలో నైట్రోజన్తో బెంజీన్ లోని కార్బన్ పరమాణువులను తొలగిం చెదరు. ఒక CH ని Nతో తొలగించడంవలన పైరిడిన్ (pyridine, C5H5N) ఏర్పడును.బెంజీన్, పైరిడిన్ నిర్మాణపరంగా సంబంధం కల్గినను, బెంజీన్ను పైరిడిన్ గా పరివర్తించడం కుదరదు.
ఉత్పత్తి మార్చు
నాలుగురకాలైన ప్రక్రియల ద్వారా ప్రాశ్రామికంగా బెంజీన్ ను ఉత్పత్తి చేయుదురు. అవి కేటలైటిక్ రిఫార్మింగు, టోలిన్ హైడ్రోడిఅల్కలైసన్ (toluene hydrodealkylation) టోలిన్ డిస్ప్రొపోర్షనేసన్ (toluene disproportionation), స్టీమ్ క్రాకింగ్.1978, 1981మధ్యలో అమెరికాలో ఉత్పత్తి కావింపబడిన బెంజీన్లో కేటలైటిక్ రిఫార్మింగు విధానప్రక్రియ పద్ధతిలో 45-50% వరకు బెంజీన్ ఉత్పత్తి చేయబడింది.
కేటలైటిక్ రిఫార్మింగు మార్చు
కేటలైటిక్ రిఫార్మింగు విధానంలో 60–200 °Cమధ్య మరుగు స్థానం/బాష్పీ భవన స్థానం కల్గిన హైడ్రో కార్బనుల మిశ్రమానికి, హైడ్రోజన్ వాయువును మిళితం /మిశ్రితం చేసి,8-50 అట్మాస్పియరు వత్తిడిలో బై ఫంక్షనల్ ప్లాటినం క్లోరైడ్ లేదా రేనియం క్లోరైడ్ ఉత్ప్రేరకం సమక్షంలో 500–525 °Cవద్ద చర్యకులోను కావించి బెంజీన్ ను ఉత్పత్తి చేయుదురు. పైన పేర్కొన్న రసాయనచర్య పరిస్థితులలో అలిపాటిక్ హైడ్రోకార్బనులు వలయాకృతి హైడ్రోకార్బనులుగా పరివర్తన చెందును., హైడ్రోజన్ పరమాణువులను కోల్పోయి ఆరోమాటిక్ హైడ్రోకార్బనులను ఏర్పరచును. రసాయనచర్య ఫలితంగా ఏర్పడిన ఆరోమాటిక్ హైడ్రోకార్బనులను డైఇథైలిన్ గ్లైకోల్ లేదా సల్ఫోలేన్ (sulfolane) వంటి ద్రావణి (solvent) లను ఉపయోగించి వేరుచేయుదురు.తరువాత స్వేదనప్రక్రియ ద్వారా (distillation) బెంజీన్ను మిగతా ఆరోమాటిక్ హైడ్రోకార్బనులనుండి వేరుచేయుదురు.
టోలిన్ హైడ్రోడిఅల్కైలెసన్(Toluene hydrodealkylation) మార్చు
ఈ విధానంలో టోలిన్ ను బెంజీన్ గా పరివర్తించెదరు.మొదట టోలిన్ ను హైడ్రోజన్ వాయువుతో మిళితం చేసి, 40–60 అట్మాస్పియరు వత్తిడిలో 500–600 °C ఉష్ణోగ్రత వద్ద క్రోమియం, మాలిబ్డినం, లేదా ప్లాటినం ఆక్సైడ్ ఉత్ప్రేరకం మీదుగా ప్రసరింప చేయుదురు.చర్యాఫలితంగా టోలిన్ డిఅల్కైలెసన్కు లోనై బెంజీన్, మిథేన్ను ఏర్పరచును.
- C6H5CH3 + H2 → C6H6 + CH4
ఇది తిరోగామిచర్య కావడం వలన అత్యధిక ఉష్ణోగ్రతలో సమతుల్యత పార్శరసాయన చర్య కారణంగా బైఫెనైల్ ను ఏర్పరచును.
- 2 C
6H
6 H
2 + C
6H
5–C
6H
5
- 2 C
చర్యలోఉపయోగించు ముడి పదార్థాలలో ఆరోమాటిక్ కాని సంఘటన పదార్థాలు/అంశీభూతాలు (పారాఫిన్లు, నాప్తేనులు) ఎక్కువ ప్రమాణంలో ఉన్నచో తక్కువ పొడవున్న (తక్కువ కార్బనులను కల్గిన) మిథేనులు ఏర్పడును, తత్ఫలితంగా ఎక్కువ హైడ్రోజన్ చర్యలో వినియోగింపబడుతుంది.ఈ విధానంలో 95% వరకు ఉత్పాదితాలను పొందవచ్చును.కొన్ని సార్లు టోలిన్ బదులుగా క్సైలెన్ (xylenes ) లను ఉపయోగించినప్పటికీ, మంచి ఫలితాలే పొందవచ్చును.
టోలిన్ డిస్ప్రొపోరసనేసన్(Toluene disproportionation) మార్చు
బెంజీన్, క్సైలిన్ (xylene) లు రెండు కూడా ఉత్పాదితాలుగా (products) అవసరమైనప్పుడు టోలిన్ డిస్ప్రొపోరసనేసన్ విధానాన్ని అనుసరిస్తారు.రెండు టోలిన్ అణువులు పరస్పరం చర్యలో పాల్గొని, వాటి అణువులోని మిథైల్ గ్రూప్లు పునఃఅమరిక చెందటం వలన ఒక అణువు బెంజీన్, ఒక అణువు క్సైనెన్ ఏర్పడును.మామూలు ఇతర క్సైలెన్ ఐసోమర్ లకన్నపారా-క్సైలెన్ (p-xylene) ఉత్పత్తి అవసరమై నప్పుడు, సెలెక్టివ్ టోలిన్ డిస్ప్రొపోరసనేసన్ విధానం ఉపయోగిస్తారు.
స్టీమ్ క్రాకింగ్ మార్చు
స్టీమ్ క్రాకింగ్ అను ప్రక్రియ ద్వారా అలిపాటిక్ హైడ్రోకార్బన్లనుండి ఇథైలిన్, ఇతర ఆల్కినులను ఉత్పత్తి చేస్తారు.ఒలిఫినులను ఉత్పత్తిచేయు ఈ స్టీమ్ క్రాకింగ్ ప్రక్రియలో వాడు ఫీడ్ స్టాక్ను బట్టి, బెంజీన్ను అధిక ప్రమాణంలో కల్గిన పైరోలైసిస్ గ్యాసోలిన్ (pyrolysis gasoline) ఉత్పత్తిచేయవచ్చును.
ఇతర సంశ్లేషణ విధానాలు మార్చు
వ్యాపారశైలిలో కాకున్నను బెంజీన్ను ఉత్పత్తి కావించు ఇతర ప్రక్రియలు పలురకాలు ఉన్నాయి. లోహాల ద్వారా ఫెనోల్, హలోబెంజిన్లను క్షయికరించడం ద్వారా కూడా బెంజీన్ను ఉత్పత్తి కావించవచ్చును. బెంజోయిక్ ఆసిడ్, దాని లవణాలను డికార్బోక్సిలేసన్ చెయ్యడం వలన బెంజీన్ను ఉత్పత్తి చేయవచ్చును. డైఅజోనియం సమ్మేళన/సంయోగ పదార్థం ద్వారా హైపో ఫాస్పరస్ఆమ్లంతో అనిలైన్ (aniline) రసాయన చర్యవలన కూడాబెంజీన్ ఏర్పడును. అలాగే ఎసిటిలిన్ను ట్రైమెరిజేసన్ చెయ్యడం వలన కూడా బెంజీన్ను ఉత్పత్తి చేస్తారు.
ఉపయోగాలు మార్చు
పలురకాల రసాయన సంయోగ పదార్థాలను తయారు చేయుటలో బెంజీన్ను మధ్యస్థాయి (intermediate) రసాయనపదార్థంగా విరివిగా ఉపయోగిస్తారు. ఇథైల్ బెంజీన్, కుమేన్, సైక్లో హెక్సేన్, అల్కైల్ బెంజీన్ లను బెంజీన్ నుండే ఉత్పత్తి చేస్తారు. పాలీమర్లు, పాలిస్టిరెన్ వంటి ప్లాస్టిక్లతయారికి మూలమైన స్టైరెన్ (styrene) ఉత్పత్తికి పూర్వగామి (precursor) అయిన ఇథైల్ బెంజీన్ ఉత్పత్తికే అత్యధికమగా బెంజీన్ ను ఉపయోగిస్తారు.20% బెంజీన్ను కుమేన్ (cumene) ఉత్పత్తికి ఉపయోగిస్తారు.కుమేన్ నుండి రెసిన్, జిగురుపదార్థాలలు/ అతుకుడు పదార్థాల (adhesives) లోవాడు ఫెనోల్, అసిటోన్ లను ఉత్పత్తి చేస్తారు. ప్రపంచవ్యాప్త బెంజీన్ ఉత్పత్తిలో 10% వరకు నైలాన్ ఫైబరులను ఉత్పత్తికి వాడుచున్నారు. నైలాన్ను వస్త్రపరిశ్రమలలో, ఇంజనీరింగు ప్లాస్టిక్లలో వాడెదరు.తక్కువ స్థాయిపరిమాణంలో కొన్ని రకాల రబ్బరును, కందెన లను, అద్దకపు రంగులను, డెటర్జంట్లను, డ్రగ్స్ను, ప్రేలుడుపదార్థాలను, క్రిమి సంహారకమందుల తయారిలో ఉపయోగిస్తారు. మధ్య తూర్పుదేశాలలో, ఆఫ్రికాలో బెంజీన్ ఉత్త్పత్తి పెరిగింది. ప్రస్తుతం తరచుగా టోలిన్ ను బెంజీన్కు ప్రత్యామ్నాయగా, ఇంధనపు అడిటివ్ గా చేర్చుచున్నారు. బెంజీన్, టోలిన్ల ద్రావణి లక్షణాలు సమానమైనప్పటికి, బెంజీన్ కన్న టోలిన్ తక్కువ విషగుణం కల్గిఉన్నది.
గాసోలిన్లో అంశీభూత పదార్థంగా మార్చు
1950 కి ముందు గ్యాసోలిన్ (పెట్రోల్) లో దాని యొక్క అక్టేన్రేటింగును పెంచుటకు, నాకింగును (knocking) తగ్గించుటకు బెంజీన్ను అధికమొత్తంలో కలిపేవారు.అంటినాకింగ్ ఏజెంట్గా టెట్రాఇథైల్ లెడ్ ను వాడటం మొదలైనాక, బెంజీన్ వాడకం ఆగిపోయింది.అయితే వాతావరణంలో సీసము (మూలకము) /లెడ్ పరిమాణం పై వివాదం కారణంగా, పెట్రోల్లో మళ్ళి బెంజీన్ వాడకం కొన్ని దేశాలలో మొదలైనది. గ్యాసోలిన్లో బెంజీన్ శాతాన్ని 0.6-1% వరకు మాత్రమే వాడటానికి అనుమతినియంత్రణ ఉంది.
రసాయన చర్యలు మార్చు
బెంజీన్ యొక్క సామాన్య రసాయన చర్య ప్రోటాన్ను ఇతర సమూహాలలో ప్రతిస్థాపన/బదులుగా పెట్టుట (substitution) చేయడం.
సల్ఫోనేసన్,క్లోరినేసన్,నైట్రెసన్ మార్చు
ఎలక్ట్రో ఫిలిక్ ఆరోమాటిక్ ప్రతిస్థాపన (బదులుగా పెట్టుట :substitution) విధానాని ఉపయోగించి బెంజీన్ ఫ్రేం వర్కులో చాలా ఫంక్షనల్ గ్రూపులను అనుసంధానించ వచ్చును.బెంజీన్ను సల్ఫోనేసన్ వలన ఉపయోగ కరమైన డెటర్జెంట్లు ఏర్పడును.బెంజీన్ నైట్రేసన్ వలన బెంజీన్ నైట్రోనియమ అయాన్ (NO2+) తో చర్య జరుపును. నైట్రోనియమ అయాన్ అనునది సల్ఫ్యూరిక్ ఆమ్లం, నైట్రిక్ ఆమ్లాలను కలపడం వలన ఏర్పడిన బలమైన ఎలక్ట్రాన్ఆకర్షణి (electrophile). నైట్రోబెంజీన్ అనునది అనిలైన్ (aniline) రసాయన ఉత్పత్తికి పూర్వగామిగా పనిచేయును. ఇక క్లోరినేసన్ అను చర్య అల్యూమినియం ట్రైక్లోరైడ్ ఉత్ప్రేరకం సమక్షలో క్లోరిన్ బెంజీన్తో కలయడం వలన క్లోరోబెంజీన్ ఏర్పడును.
హైడ్రోజనేసన్ మార్చు
బెంజీన్ను ఉదజనికరణ (hydrogenation) కావించడం వలన సైక్లోహెక్సేన్, ఇతర బెంజీన్ వుత్పన్నపదార్థాలు ఏర్పడును.బాగా చూర్ణంవల్లే చేయబడిన నికెల్ ఉత్ప్రేరకంసమక్షంలో, అధికవత్తిడి వద్ద బెంజీన్తో హైడ్రోజన్ వాయువును చర్యకులోను కావించడం వలన సైక్లోహేక్సేన్, ఇతర బెంజీన్ వుత్పన్నపదార్థాలు (derivatives) ఏర్పడును.ఉత్ప్రేరకం లేనిచో బెంజీన్ అంత చురుకుగా చర్యలో పాల్గొనదు. ఈ విధానంలో పారిశ్రామికంగా భారి ప్రమాణంలో ఉత్పత్తి చేయుదురు.
ఆరోగ్రం పై ప్రభావం మార్చు
బెంజీన్ వలన క్యాన్సర్, ఇతర రోగాలు కలుగు అవకాశాలు కలదు[16].ముఖ్యంగా ఎముక లలోని మూలుగ పాడైపోవుటకు బెంజీన్ మూల హేతువు.అవికసితం పాండురోగం (అపలస్టిక్ అనేమియా), లుకేమియా, మూలుగలోని అసామాన్య లక్షణాలు బెంజీన్ ప్రభావానికి లోనైనందున కలుగును.[13] బెంజీన్ గ్యాసోలిన్లో, ఇతర హైడ్రోకార్బన్లలో ఉండటం వలన ప్రపంచవ్యాప్తంగా మనుష్యులు బెంజీన్ ప్రభావానికి తప్పనిసరిగా లోనవుతారు.అందు వలన ఇది ప్రపంచ ఆరోగ్య సమస్య.బెంజీన్ కాలేయం, మూత్రపిండాలు, ఊపిరి తిత్తులు, గుండె, మెదడు పై తన విషప్రభావాన్ని చూపించును. బెంజీన్ జంతువులలో, మనుషులలో క్యాన్సరు కల్గించు అవకాశం ఉంది.బెంజీన్ ఆవిరులను అధిక మోతాదులో ఎక్కువ కాలం శ్వాసించిన కొందరు స్త్రీలలో రుతుకాలం అనియంత్రణ (రుతుస్రవంలో మార్పులు) చెందటం, అండాశయంలోని అండాల పరిమాణం తగ్గడం వంటి పరిణామాలు చోటు చేసుకొనును.ఎక్కువ ప్రమాణంలో బెంజీన్ ప్రభావానికి గురైన పురుషులలో, శుక్ర కణాల్లో అసాధారణ ప్రమాణంలో క్రోమోజోములను గుర్తించారు.దీని కారణంగా పిండఫలదీకరణ పై, పిండ అభివృద్ధి/ఎదుగుదల పై ప్రభావం చూపును.
బెంజీన్ ప్రభావానికి గురైన కలుగు ఫలితాలు మార్చు
ఏజెన్సి ఫర్ టాక్సిక్ సబ్ స్టేన్సస్ అండ్ డిసిజ్ రిజిస్ట్రి (ATSDR)2007 ప్రకారం బెంజీన్ స్వాభావికంగా జరుగు రసాయన ప్రక్రియలవల, anthropogenically ఉత్పత్తి అగును. స్వాభావికంగా జరుగు రసాయన ప్రక్రియలు అనగా అగ్ని పర్వతాల విస్పొటన, దావాగ్ని వలన, ఫెనోల్ వంటి రసాయన పదార్థాలను సంశ్లేషణచేయునపుడు, సింథటిక్ ఫైబరులను, ఉత్పత్తి చేయునపుడు, రబ్బరును ఫాబ్రికేసన్ చేయునపుడు, ఇంకా కందెనలు, క్రిమి సంహారకమందులను తయారు చేయునపుడు, వైద్యపరమైన మందుల తయారీలో, అద్దకపురంగులను తయారు చేయునపుడు బెంజీన్ పరిసరాలలో విడుదల అగును.బెంజీన్ ప్రభావం కల్గించు ముఖ్య వనరులు పొగాకు నుండి వెలువడు పొగ, అటోమొబైల్ స్టేషన్లలో, వాహనాలనుండి వెలువడు పొగలో, పారిశ్రామిక వాడలనుండి వెలువడు ఉద్గారాలు (emissions) [13].కలుషిత నీటితో సంపర్కం వలన కూడా బెంజీన్ జీర్ణకోశం ద్వారా లేదా చర్మం ద్వారా దేహవ్యవస్థలో చేరును.
దేహంలో చేరిన బెంజీన్ hepatically జీర్ణ /దేహప్రక్రియకు/పచన క్రియకు (metabolize) లోనై, మూత్రం ద్వారా విసర్జింపబడును.
మూలాలు/ఆధారాలు మార్చు
- ↑ Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics (86th ed.). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ↑ Arnold, D.; Plank, C.; Erickson, E.; Pike, F. (1958). "Solubility of Benzene in Water". Industrial & Engineering Chemistry Chemical & Engineering Data Series. 3 (2): 253–256. doi:10.1021/i460004a016.
- ↑ Breslow, R.; Guo, T. (1990). "Surface tension measurements show that chaotropic salting-in denaturants are not just water-structure breakers". Proceedings of the National Academy of Sciences of the United States of America. 87 (1): 167–9. Bibcode:1990PNAS...87..167B. doi:10.1073/pnas.87.1.167. PMC 53221. PMID 2153285.
- ↑ Coker, A. Kayode; Ludwig, Ernest E. (2007). Ludwig's Applied Process Design for Chemical And Petrochemical Plants. Vol. 1. Elsevier. p. 114. ISBN 0-7506-7766-X.
- ↑ 5.0 5.1 5.2 5.3 5.4 http://chemister.ru/Database/properties-en.php?dbid=1&id=644
- ↑ 6.0 6.1 Atherton Seidell; William F. Linke (1952). Solubilities of Inorganic and Organic Compounds: A Compilation of Solubility Data from the Periodical Literature. Supplement. Van Nostrand.
- ↑ 7.0 7.1 7.2 మూస:Nist
- ↑ 8.0 8.1 8.2 Sigma-Aldrich Co., Benzene. Retrieved on 2014-05-29.
- ↑ 9.0 9.1 9.2 NIOSH Pocket Guide to Chemical Hazards. "#0049". National Institute for Occupational Safety and Health (NIOSH).
- ↑ "Benzene". Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ↑ "What is Benzene?". study.com/academy. Retrieved 2016-05-02.
- ↑ "Facts About Benzene". bt.cdc.gov. Archived from the original on 2010-09-02. Retrieved 2016-05-02.
- ↑ 13.0 13.1 13.2 "Benzene". pubchem.ncbi.nlm.nih.gov. Retrieved 2016-05-02.
- ↑ "Benzene (C6H6)". britannica.com. Retrieved 2016-05-02.
- ↑ "EXPOSURE TO BENZENE:" (PDF). who.int. Retrieved 2016-05-02.
- ↑ "Benzene and Cancer Risk". cancer.org. Archived from the original on 2016-04-30. Retrieved 2016-05-02.