అమ్మోనియం సైనైడ్
అమ్మోనియం సైనైడ్ ఒక రసాయనిక సంయోగ పదార్థం. ఇది అస్థిరమైన అకర్బన సమ్మేళన పదార్థం. ఈ సంయోగ పదార్థం యొక్క రసాయనిక ఫార్ములా NH4CN.
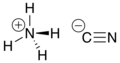
| |||
| |||
| గుర్తింపు విషయాలు | |||
|---|---|---|---|
| సి.ఎ.ఎస్. సంఖ్య | [12211-52-8] | ||
| పబ్ కెమ్ | 159440 | ||
| SMILES | [C-]#N.[NH4+] | ||
| |||
| ధర్మములు | |||
| NH4CN | |||
| మోలార్ ద్రవ్యరాశి | 44.0559 g/mol | ||
| స్వరూపం | colourless crystalline solid | ||
| సాంద్రత | 1.02 g/cm3 | ||
| బాష్పీభవన స్థానం | 36 °C (97 °F; 309 K) | ||
| very soluble | |||
| ద్రావణీయత | very soluble in alcohol | ||
| సంబంధిత సమ్మేళనాలు | |||
| ఇతరఅయాన్లు | {{{value}}} | ||
ఇతర కాటయాన్లు
|
Sodium cyanide Potassium cyanide | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |||
| Infobox references | |||
భౌతిక ధర్మాలు
మార్చుఅమ్మోనియం సైనైడ్ ఒక రంగులేని చతుర్క్కోణ స్పటిక ఘన పదార్థం.[1] ఈ సంయోగ పదార్థం యొక్క అణుభారం 44.055 గ్రాములు/మోల్.[2] అమ్మోనియం సైనైడ్ సాంద్రత 1.02 గ్రాములు/సెం.మీ3. ఈ సంయోగ పదార్థం యొక్క భాస్పిభవన ఉష్ణోగ్రత 36 °C. అమ్మోనియం సైనైడ్నీటిలో, ఆల్కహాల్లో కరుగుతుంది.
రసాయన చర్యలు
మార్చుఅమ్మోనియం సైనైడ్ వియోగం చెందడం వలన అమ్మోనియా, హైడ్రోజన్ సైనైడ్ ఏర్పడును. వియోగ ఫలితంగా తరచుగా నల్లని హైడ్రోజన్ సైనైడ్ పాలిమర్ ఏర్పడును.
- NH4CN → NH3 + HCN
అమ్మోనియం సైనైడ్ ద్రావణం లోహ లవణాలతో చర్య వలన ఉభయ వియోగం చెందును. గ్లైఅక్షల్ (glyoxal) తో చర్య వలన అమినోఅసిటిక్ ఆమ్లాన్ని (glycine) ఏర్పరచును.
- NH4CN + (CHO)2 → NH2CH2COOH + HCN
అలాగే కిటోన్సుతో చర్య ఫలితంగా అమినో నైట్రైల్స్ (aminonitriles) ఏర్పరచును.
- NH4CN + CH3COCH3 → NH2CH2CH2CH2CN + H2O
ఉత్పత్తి
మార్చుతక్కువ ఉష్ణోగ్రత వద్ద సజల అమ్మోనియాలో హైడ్రోజన్ సైనైడ్ను బబ్లింగ్ చెయ్యడం ద్వారా అమ్మోనియం సైనైడ్ను ఉత్పత్తి చెయ్యుదురు.
- HCN + NH3(aq) → NH4CN(aq)
కాల్షియం సైనైడ్ తో అమ్మోనియం కార్బోనేట్ రసాయనిక చర్య జరిపిన అమ్మోనియం సైనైడ్ఏర్పడును.
- Ca(CN)2 + (NH4)2CO3 → 2 NH4CN + CaCO3
పొడి (dry) స్థితిలో ఉన్న పొటాషియం సైనైడ్ లేదా పొటాషియం పెర్రో సైనైడ్,, అమోనియం క్లోరైడ్ మిశ్రమాన్ని వేడి చేసి, ఆవిరి రూపంలో వెలువడిన అమ్మోనియం సైనైడ్ను స్పటికాలుగా మారునట్లు చల్లార్చటం ద్వారా కూడాతయారు చెయ్య వచ్చును.
- KCN + NH4Cl → NH4CN + KCl
విష స్వభావం
మార్చుఅమ్మోనియం సైనైడ్ ద్రవంగా లేదా ఘన పదార్థంగా అత్యంత విషకారి.జీర్ణాశయంలో చేరిన మరణం సంభవించును. ఘన రూప అమ్మోనియం సైనైడ్ ప్రభావానికి గురైన ఇది అత్యంత ప్రమాదకరమైన హైడ్రోజన్ సైనైడ్,, అమ్మోనియాగా విఘటన చెందటం వలన చాలా ప్రమాదకరం.
రసాయన విశ్లేషణ
మార్చుఅమ్మోనియం సైనైడ్లో ఉన్న మూలకాల నిష్పతి :హైడ్రోజన్ ( H) : 9.15%, కార్బన్ (C) : 27.23%, నత్రజని (N) : 63.55%.
మూలాలు
మార్చు- ↑ "Ammonium Cyanide". matweb.com. Retrieved 2015-07-27.
- ↑ "Ammonium Cyanide". pubchem.ncbi.nlm.nih.gov. Retrieved 2015-07-27.

