ద్రవ్యనిత్యత్వ నియమం
ద్రవ్యరాశి నిత్యత్వ నియమం ప్రకారం పదార్థం, శక్తి బదిలీలు జరగని మూసివేయబడిన ఏ వ్యవస్థలోనైనా, వ్యవస్థ ద్రవ్యరాశి స్థిరంగా ఉంటుంది. ఎందుకంటే వ్యవస్థ ద్రవ్యరాశి మారదు. ద్రవ్యరాశి పరిమాణం కాలక్రమేణా నిత్యత్వం చెందుతుంది. ద్రవ్యరాశి అంతరిక్షంలో పునర్వ్యవస్థీకరించినప్పటికీ, లేదా దానితో సంబంధం ఉన్న పదార్థాలు రూపంలో మార్చగలిగినప్పటికీ, ద్రవ్యరాశిని సృష్టించలేము లేదా నాశనం చేయలేమని ఈ నియమం తెలుపుతుంది. ఉదాహరణకు రసాయన చర్యలో క్రియాజనకాల ద్రవ్యరాశి, క్రియా జన్యాల ద్రవ్యరాశికి సమానంగా ఉంటుంది.
కట్టె బొగ్గును మండిస్తే దాని భారం తగ్గుతుందని చాలా కాలం భావించడం జరిగింది. కానీ లావోయిజర్ కట్టె బొగ్గును మండించినపుడు ఏర్పడే పదార్థం ఏదీ కూడా బయటకు పోకుండా మూసి ఉన్న ఏర్పాటుతో ప్రయోగం ఛేసినపుడు మొత్తం భారంలో ఏ మార్పు గమనించలేదు. ఈ పరిశీలన ఆధారంగా లెవోయిజర్ కీంది ద్రవ్యనిత్యత్వ నియమాన్ని ప్రతిపాదించాడు.
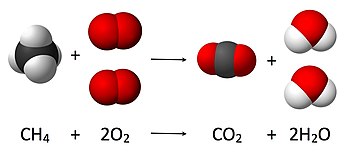
" ఒక రసాయన చర్యలో (ద్రవ్యరాశిని) సృష్టించలేం, నాశనం చేయలేం" మరో విధంగా చెప్పాలంటే "ఒక రసాయన చర్యలో ఏర్పడిన క్రియాజన్యాల ద్రవ్యరాశి ఆ చర్యలో పాల్గొన్న క్రియా జనకాల ద్రవ్యరాశికి సమానం"
ద్రవ్యనిత్యత్వ నియమాన్ని లెవోయిజర్ ప్రతిపాదించినప్పటికీ దీనిని లాండాల్ట్ అనే శాస్త్రవేత్త అభివృద్ధి చెందిన పరికరాలతొ ప్రయోగం చేసి ఋజువు చేసాడు. బాహ్య వ్యవస్థలలో ద్రవ్యరాశి నిత్యత్వం చెందబడదు.
చరిత్ర
మార్చుద్రవ్యరాశి నిత్యత్వ నియమాన్ని 1748 లోమిఖాయిల్ లోమోనోసోవ్ (1711–1765) మొదట వివరించాడు. అతను దీనిని ప్రయోగాల ద్వారా నిరూపించాడు. అయినప్పటికీ ఇది కొన్నిసార్లు సవాలు చేయబడింది[1]. ఆంటోయిన్ లావోసియర్ (1743–1794) ఈ ఆలోచనలను 1774 లో వ్యక్తం చేశాడు. లావోసియర్ యొక్క పరిశోధనకు ముందే జోసెఫ్ బ్లాక్ (1728–1799), హెన్రీ కావెండిష్ (1731–1810), జీన్ రే (1583–1645) లు కూడా పరిశోధనలు చేసారు[2].
మూలాలు
మార్చు- ↑ * Pomper, Philip (1962). "Lomonosov and the discovery of the law of the conservation of matter in chemical transformations". Ambix. 10 (3): 119–127.Lomonosov, Mikhail Vasil’evich (1970). Mikhail Vasil’evich Lomonosov on the corpuscular theory. Henry M. Leicester (transl.). Cambridge, Mass.: Harvard University Press. Introduction, p. 25.
- ↑ [1]. Whitaker, Robert D. 1975. Journal of Chemical Education, 52 (10) 658-659.