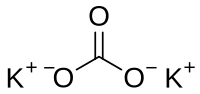
పొటాషియం కార్బోనేట్
| |
| |

| |
| పేర్లు | |
|---|---|
| IUPAC నామము
Potassium carbonate
| |
| ఇతర పేర్లు
Carbonate of potash, Dipotassium carbonate, Sub-carbonate of potash, Pearl ash, Potash, Salt of tartar, Salt of wormwood.
| |
| గుర్తింపు విషయాలు | |
| సి.ఎ.ఎస్. సంఖ్య | [584-08-7] |
| పబ్ కెమ్ | 11430 |
| ఆర్.టి.ఇ.సి.యస్. సంఖ్య | TS7750000 |
| SMILES | C(=O)([O-])[O-].[K+].[K+] |
| |
| ధర్మములు | |
| K2CO3 | |
| మోలార్ ద్రవ్యరాశి | 138.205 g/mol |
| స్వరూపం | white, hygroscopic solid |
| సాంద్రత | 2.43 g/cm3 |
| ద్రవీభవన స్థానం | 891 °C (1,636 °F; 1,164 K) |
| బాష్పీభవన స్థానం | decomposes |
| 112 g/100 mL (20 °C) 156 g/100 mL (100 °C) | |
| ద్రావణీయత | insoluble in alcohol, acetone |
| ప్రమాదాలు | |
| ప్రధానమైన ప్రమాదాలు | Irritant |
| R-పదబంధాలు | R22 R36 R37 R38 |
| జ్వలన స్థానం | {{{value}}} |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
1870 mg/kg (oral, rat)[1] |
| సంబంధిత సమ్మేళనాలు | |
| ఇతరఅయాన్లు | {{{value}}} |
ఇతర కాటయాన్లు
|
Lithium carbonate Sodium carbonate Rubidium carbonate Caesium carbonate |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |
| Infobox references | |
ప్రాథమిక సమాచారం
మార్చుపొటాషియం కార్బోనేట్ (K2CO3) తెల్లని లవణం.పొటాషియం మూలకం యొక్క సమ్మేళనం.
చరిత్ర
మార్చుఅంటోనియో క్యాంపనెల్ల (Antonio Campanella) అను రాసాయన శాస్త్రవేత్త 1742 లో ఈ సమ్మేళనాన్ని గుర్తించాడు.మొదటి అమెరికాదేశపు పేటెంట్ హక్కు 1790 లో అభివృద్ధిపరచిన పొటాషియం, పెరల్ యాష్ తయారు చేయు పద్ధతికి శామ్యూల్ హాప్ కిన్స్ అనే అతనికి దక్కినది.18 వశతాబ్ది చివరలో బెకింగు పౌడరును అభివృద్ధి చెయ్యుటకు ముందు పెరల్ యాష్ను క్విక్ బ్రేడ్సు (సత్వర రొట్టెలు) లో గుల్లతనం కల్గించు ఏజెంటుగా వాడేవారు.
భౌతిక లక్షణాలు
మార్చుపొటాషియం కార్బోనేట్ తెల్లని స్పటిక రూప ఘనపదార్థం.ఇది నీటిలో కరుగుతుంది.కాని ఇథనాల్, అసిటోన్ లలో కరుగదు.నీటిలో కరగడం వలన గాఢ క్షార ద్రావణం ఏర్పడును.పొటాషియం హైడ్రోక్సైడ్ తో కార్బన్ డై ఆక్సైడ్బొగ్గుపులుసు వాయువుతో శోషణచర్య వలన పొటాషియం కార్బోనేట్ ఏర్పడును.పొటాషియం కార్బోనేట్ బయలు గాలిలో ఉంచిన ద్రవించు, చెమ్మగిల్లు లక్షణం కలిగి యున్నది. పోటాషియం కార్బోనేట్ ను సబ్బుల తయారి, గాజు తయారీలో ఉపయోగిస్తారు.పొటాషియం కార్బోనేట్ యొక్క సాంద్రత:2.43 గ్రాములు/సెం.మీ3.ద్రవీభవన స్థానం 891 °C.20 °C వద్ద ద్రావణీయత 112 గ్రాములు,100 మి.లీ నీటిలో. 100 °C వద్ద ద్రావణియత 156 గ్రాములు 100 మి.లీ నీటిలో.
ఉత్పత్తి
మార్చువర్తమానకాలంలో వాణిజ్య పరంగా పొటాషియం క్లోరైడును విద్యుద్విశ్లేషణ చేయ్యుట ద్వారా ఉత్పత్తి చేస్తున్నారు.విదుద్విశ్లేషణ వలన ఏర్పడిన పొటాషియం హైడ్రాక్సైడ్కు కార్బన్ డై అక్సైడుతో చర్య జరిపించ డం వలన పొటాషియం కార్బోనేట్ ఏర్పడును.ఈ విధంగా ఏర్పడిన పొటాషియం కార్బోనేట్ ను ఇతర పొటాషియం సమ్మెళనాలను ఉత్పత్తి చెయ్యుటకు ఉపయోగిస్తారు.
- 2KOH + CO2 → K2CO3 + H2O
వినియోగం
మార్చు- సబ్బులు, గాజు, పింగాణి వస్తువుల తయారీలో ఉపయోగిస్తారు.
- డ్రైయింగ్ ఏజెంట్ గా ఉపయోగిస్తారు
- వంటకాల తయారిలో గ్రాస్ జెల్లిగా ఉపయోగిస్తారు.
- కోకో పౌడరును ఉత్పత్తి చెయ్యునప్పుడు, పౌడరు యొక్క pH (ఉదజని సంభావ్యత) ని సమతుల్యంలో ఉంచుట కై ఉపయోగిస్తారు.
- షర్బత్తు, మధువు, తయారు చెయ్యునప్పుడు దీనిని బఫరింగు ఏజెంట్ గా ఉపయోగిస్తారు.
- కఠినజలాన్ని సాధుజలంగా పరివర్తించుటకు వాడెదరు.
- అగ్ని ప్రమాద సమయంలో B –కేటగిరికి చెందిన మంటలను ఆర్పు అగ్నినిరోధక పరికారాలలో ఉపయోగిస్తారు.
- మెటల్ ఆర్కు వెల్డింగులో ఉపయోగించు వెల్డింగ్ ఎలక్ట్రోడు లా ఉపరితలంపై ఉపయోగించు పూరకం (Flux ) పదార్థా లలో పొటాషియం కార్బోనేట్ ను ఉపయోగిస్తారు.
- న్యూరాన్స్ సమతుల్యం ఉండుటకై పొటాషియం కార్బోనేట్ అవసరం.
- పెంపుడు జంతువులలో పౌష్టిక ఆహారంలో పొటాషియం లోపం రాకుండుటకై పొటాషియం కార్బోనేట్ను కలుపుతారు.