బొరాన్ ట్రైఆక్సైడ్
బోరాన్ ట్రైఆక్సైడ్ ఒక అకర్బన రసాయన సమ్మేళన పదార్ధం.దీనిని డైబోరాన్ ట్రైఆక్సైడ్ అనికూడా అంటారు.బోరాన్ యొక్క ఆక్సైడ్ సంయోగపదార్థాలలో ఇది యొకటి.బోరాన్, ఆక్సిజన్ మూలకాల పరమాణువుల సంయోగం వలన ఈసంయోగ పదార్థం రూపుదిద్దుకున్నది.

| |
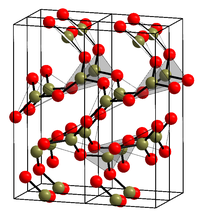
| |
| పేర్లు | |
|---|---|
| ఇతర పేర్లు
boron oxide, diboron trioxide, boron sesquioxide, boric oxide, boria
Boric acid anhydride | |
| గుర్తింపు విషయాలు | |
| సి.ఎ.ఎస్. సంఖ్య | [1303-86-2] |
| పబ్ కెమ్ | 518682 |
| యూరోపియన్ కమిషన్ సంఖ్య | 215-125-8 |
| సి.హెచ్.ఇ.బి.ఐ | CHEBI:30163 |
| ఆర్.టి.ఇ.సి.యస్. సంఖ్య | ED7900000 |
| SMILES | O=BOB=O |
| |
| ధర్మములు | |
| B2O3 | |
| మోలార్ ద్రవ్యరాశి | 69.6182 g/mol |
| స్వరూపం | white, glassy solid |
| సాంద్రత | 2.460 g/cm3, liquid; 2.55 g/cm3, trigonal; |
| ద్రవీభవన స్థానం | 450 °C (842 °F; 723 K) (trigonal) 510 °C (tetrahedral) |
| బాష్పీభవన స్థానం | 1,860 °C (3,380 °F; 2,130 K) ,[1] sublimates at 1500 °C |
| 1.1 g/100mL (10 °C) 3.3 g/100mL (20 °C) 15.7 100 g/100mL (100 °C) | |
| ద్రావణీయత | partially soluble in methanol |
| ఆమ్లత్వం (pKa) | ~ 4 |
| అయస్కాంత ససెప్టిబిలిటి | -39.0·10−6 cm3/mol |
| ఉష్ణగతిక రసాయన శాస్త్రము | |
| నిర్మాణము మారుటకు కావాల్సిన ప్రామాణిక ఎంథ్రఫీ ΔfH |
-1254 kJ/mol |
| ప్రామాణిక మోలార్ ఇంథ్రఫీ S |
80.8 J/mol K |
| విశిష్టోష్ణ సామర్థ్యం, C | 66.9 J/mol K |
| ప్రమాదాలు | |
| ప్రధానమైన ప్రమాదాలు | |
| ఇ.యు.వర్గీకరణ | {{{value}}} |
| జ్వలన స్థానం | {{{value}}} |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
3163 mg/kg (oral, mouse)[3] |
| US health exposure limits (NIOSH): | |
PEL (Permissible)
|
TWA 15 mg/m3[2] |
REL (Recommended)
|
TWA 10 mg/m3[2] |
IDLH (Immediate danger)
|
2000 mg/m3[2] |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |
| Infobox references | |
ఉత్పత్తి
మార్చుకరిగించు కొలిమిలో బోరాక్సు, సల్ఫ్యూరిక్ ఆమ్లం మధ్య రసాయనచర్య వలన బోరాన్ ట్రైఆక్సైడ్ ఏర్పడును.750°C వద్ద కరిగిన ,ద్రవస్థితి బోరాన్ ఆక్సైడ్ సోడియం సల్ఫేట్ నుండి వేరు పడును.దీనిని తేర్చి(decanted),చల్లార్చిన 96–97% శుద్ధత కల్గిన బోరాన్ ట్రైఆక్సైడ్ ఉత్పత్తి అగును.
మరొక పద్ధతిలో బోరిక్ ఆమ్లాన్ని ~300 °C లో వేడిచెయ్యడం. మొదట బొరిక్ ఆమ్లం 170 °C వద్ద నీటి ఆవిరి, మెటా బొరిక్ ఆమ్లం(HBO2)గా ఏర్పడును.దీనిని 300 °C వద్ద,లేదా మించి వేడిచెయ్యడం వలన అధిక నీటి ఆవిరిమరియు బోరాన్ ట్రైఆక్సైడ్ ఏర్పడును.
- H3BO3 → HBO2 + H2O
- 2 HBO2 → B2O3 + H2O
డైబోరెన్(B2H6) గాలిలోని ఆక్సిజన్తో లేదా లేదా గాలిలోని తేమతో రసాయనచర్య జరుపుట వలన కూడా బోరాన్ ట్రైఆక్సైడ్ ఉత్పత్తి చెయ్యవచ్చును.
- 2B2H6(g) + 3O2(g) → 2B2O3(s) + 6H2(g)
- B2H6(g) + 3H2O(g) → B2O3(s) + 6H2(g)
భౌతిక లక్షణాలు
మార్చుఇది తెల్లని గాజువంటి/ తళతళలాడే ఘన పదార్ధం.ఇది ఎక్కువ అనిర్దిష్ట స్ఫటికముగా ఏర్పడని రూపంలో(amorphous)లో లభించును.ఎక్కువసేపు అధికంగా annealing (వేడిచేసి కావలసిన ఆకారం లోకి మార్చి చల్లబరచడం)చెయ్యడం వలన స్పాటికాకృతి వున్న సంయోగ పదార్థ ఏర్పడును.
రుచి
మార్చుకొద్దిగా ఘాటైన రుచి కల్గి ఉన్నది.[4]
అణుభారం
మార్చుబొరాన్ ట్రైఆక్సైడ్ యొక్కఅణుభారం 69.620 గ్రాములు /మోల్[5]
సాంద్రత
మార్చుబొరాన్ ట్రైఆక్సైడ్ సాంద్రత 2.460 గ్రాములు/సెం,మీ3(ద్రవస్థితిలో)[6],త్రిభుజసౌష్టవ అణునిర్మాణ మున్న సంయోగ పదార్ధం సాంద్రత 2.55గ్రాములు/సెం.మీ3,అలాగే మొనోక్లినిక్ అణునిర్మాణ పదార్థ సాంద్రత 3.11–3.146 గ్రాములు/సెం,మీ3 మధ్య వుండును.
ద్రవీభవన ఉష్ణోగ్రత
మార్చుత్రికోణాకృతి సౌష్టవమున్న సంయోగ పదార్ధం ద్రవీభవన స్థానం 450°C (842°F;723 K)[4] కాగా చర్భుజాక్రుతి సౌష్టమున్న పదార్ధం ద్రవీభవన స్థానం 510 °C.
మరుగు ఉష్ణోగ్రత
మార్చుబోరాన్ ట్రైక్లోరైడ్ యొక్క బాష్పీభవన స్థానం/ మరుగు ఉష్ణోగ్రత 1,860°C (3,380 °F; 2,130 K).ఇది1500 °C[3]ఉష్ణోగ్రత వద్ద ఈ సంయోగ పదార్ధం ఉత్పతనం(sublimate)చెందును.[4]
ద్రావణీయత
మార్చునీటిలో కరుగుతుంది.మెథానాల్ లో పాక్షికంగా కరుగును. 10°C ఉష్ణోగ్రత వున్న100మీ.లీ నీటిలో1.1 గ్రాములు, 20°C ఉష్ణోగ్రతవున్న 100మీ.లీ నీటిలో3.3గ్రాములు, 100 C ఉష్ణోగ్రత వున్న 100మీ.లీ నీటిలో 15.71 గ్రాముల సంయోగ పదార్ధం కరుగును.
- గ్లాసు, ఎనామిల్లు లలో ఫ్లక్సింగు ఏజెంటు(Fluxing agent )గా ఉపయోగిస్తారు.
- బోరాన్ కార్బైడ్ వంటి బోరాన్ సమ్మేళనాలను తయారు చేయుటకు ప్రారంభ పదార్థంగా ఉపయోగిస్తారు.
- గ్లాసు ఫైబరులలో(ఆప్టికల్ ఫైబర్సు)లలో అదనపు చేర్పుడు పదార్థంగా ఉపయోగిస్తారు.
- బోరో సిలికేట్ గ్లాసు ఉత్పత్తిలో ఉపయోగిస్తారు.
- సేంద్రియ సంశ్లేషణలో ఆమ్ల ఉత్ర్పేరకంగా ఉపయోగిస్తారు.
ఇవికూడా చూడండి
మార్చుమూలాలు/ఆధారాలు
మార్చు- ↑ High temperature corrosion and materials chemistry: proceedings of the Per Kofstad Memorial Symposium. Proceedings of the Electrochemical Society. The Electrochemical Society. 2000. p. 496. ISBN 1-56677-261-3.
- ↑ 2.0 2.1 2.2 2.3 NIOSH Pocket Guide to Chemical Hazards. "#0060". National Institute for Occupational Safety and Health (NIOSH).
- ↑ "Boron oxide". Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ↑ 4.0 4.1 4.2 "Boric Oxide". pubchem.ncbi.nlm.nih.gov. Retrieved 2017-05-03.
- ↑ "Boron trioxide". chemspider.com. Retrieved 2017-05-03.
- ↑ "Boric anhydride". sigmaaldrich.com. Retrieved 2017-05-03.
- ↑ "Boron Oxide". reade.com. Retrieved 2017-05-03.