కార్బన్ మొనాక్సైడ్
కార్బన్ మొనాక్సైడ్ రంగు, వాసన, రుచి లేనటువంటి, గాలికన్న బరువైన వాయువు. వాతావరణంలో 35ppm మించి ఉన్నచో మనుష్యులకు ప్రమాదకరం. జీవుల, జీవ ప్రక్రియ సమయంలో అల్ప ప్రమాణంలో కార్బన్ మొనాక్సైడ్ ఉత్పత్తి అగును. కార్బన్ మొనాక్సైడ్ ఒక కార్బన్ పరమాణువు, మరో ఆక్సిజన్ పరమాణువుతో త్రిబంధ సంయోగం ఏర్పరచు కొనుట వలన ఏర్పడును. అణువు లోని త్రిబంధాలలో రెండు సమయోజనీయ బంధాలు కాగా మూడవది ద్విధ్రువ సమయోజనీయ బంధం.ఇది అతి సాధారణంగా ఆక్సోకార్బన్, సైయనైడ్ అయానులతో, నైట్రోసోనియం కేటయాన్తో,, నత్రజని అణువుతో ఐసో ఎలెక్ట్రానిక్ గా ప్రవర్తించును. సమన్వయ సంక్లిష్ట సమ్మేళనాలలో కార్బన్ మొనాక్సైడ్ లిగండ్ (ligand) ను కార్బోనైల్ అంటారు.
| |||
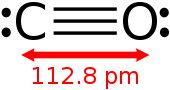
| |||
| పేర్లు | |||
|---|---|---|---|
| Preferred IUPAC name
Carbon monoxide | |||
| ఇతర పేర్లు
Carbon monooxide
Carbonous oxide Carbon(II) oxide Carbonyl Flue gas Monoxide | |||
| గుర్తింపు విషయాలు | |||
| సి.ఎ.ఎస్. సంఖ్య | [630-08-0] | ||
| పబ్ కెమ్ | 281 | ||
| యూరోపియన్ కమిషన్ సంఖ్య | 211-128-3 | ||
| కెగ్ | D09706 | ||
| వైద్య విషయ శీర్షిక | Carbon+monoxide | ||
| సి.హెచ్.ఇ.బి.ఐ | CHEBI:17245 | ||
| ఆర్.టి.ఇ.సి.యస్. సంఖ్య | FG3500000 | ||
| SMILES | [C-]#[O+] | ||
| |||
| బైల్ స్టెయిన్ సూచిక | 3587264 | ||
| జి.మెలిన్ సూచిక | 421 | ||
| ధర్మములు | |||
| CO | |||
| మోలార్ ద్రవ్యరాశి | 28.010 g/mol | ||
| స్వరూపం | colorless gas | ||
| వాసన | odorless | ||
| సాంద్రత | 789 kg/m3, liquid 1.250 kg/m3 at 0 °C, 1 atm 1.145 kg/m3 at 25 °C, 1 atm | ||
| ద్రవీభవన స్థానం | −205.02 °C (−337.04 °F; 68.13 K) | ||
| బాష్పీభవన స్థానం | −191.5 °C (−312.7 °F; 81.6 K) | ||
| 27.6 mg/L (25 °C) | |||
| ద్రావణీయత | soluble in chloroform, acetic acid, ethyl acetate, ethanol, ammonium hydroxide, benzene | ||
| kH | 1.04 atm-m3/mol | ||
| వక్రీభవన గుణకం (nD) | 1.0003364 | ||
ద్విధృవ చలనం
|
0.122 D | ||
| ఉష్ణగతిక రసాయన శాస్త్రము | |||
| నిర్మాణము మారుటకు కావాల్సిన ప్రామాణిక ఎంథ్రఫీ ΔfH |
−110.5 kJ·mol−1 | ||
| దహనక్రియకు కావాల్సిన ప్రామాణీక ఎంథ్రఫీ ΔcH |
−283.4 kJ/mol | ||
| ప్రామాణిక మోలార్ ఇంథ్రఫీ S |
197.7 J·mol−1·K−1 | ||
| విశిష్టోష్ణ సామర్థ్యం, C | 29.1 J/K mol | ||
| ప్రమాదాలు | |||
| ఇ.యు.వర్గీకరణ | {{{value}}} | ||
| R-పదబంధాలు | R61 R12 R26 మూస:R48/23 | ||
| S-పదబంధాలు | S53 S45 | ||
| జ్వలన స్థానం | {{{value}}} | ||
స్వయం జ్వలన
ఉష్ణోగ్రత |
609 °C (1,128 °F; 882 K) | ||
| విస్ఫోటక పరిమితులు | 12.5–74.2% | ||
| Lethal dose or concentration (LD, LC): | |||
LC50 (median concentration)
|
8636 ppm (rat, 15 min) 5207 ppm (rat, 30 min) 1784 ppm (rat, 4 hr) 2414 ppm (mouse, 4 hr) 5647 ppm (guinea pig, 4 hr)[1] | ||
LCLo (lowest published)
|
4000 ppm (human, 30 min) 5000 ppm (human, 5 min)[1] | ||
| US health exposure limits (NIOSH):[2] | |||
PEL (Permissible)
|
TWA 50 ppm (55 mg/m3) | ||
REL (Recommended)
|
TWA 35 ppm (40 mg/m3) C 200 ppm (229 mg/m3) | ||
IDLH (Immediate danger)
|
1200 ppm | ||
| సంబంధిత సమ్మేళనాలు | |||
| Related {{{label}}} | {{{value}}} | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |||
| Infobox references | |||
కార్బన్ కలిగిన పదార్థాలను పాక్షికంగా ఆక్సీకరణం చెయ్యడం వలన కార్బన్ మొనాక్సైడ్ వాయువును ఉత్పత్తి చెయ్యవచ్చును. కార్బన్ కలిగిన పదార్థాల లేదా సేంద్రియపదార్థాల దహనసమయంలో కార్బన్ డయాక్సైడ్ను ఉత్పత్తి చెయ్యుటకు ఆక్సిజన్ అందుబాటులో లేనప్పుడు కార్బన్ మొనాక్సైడ్ ఏర్పడును.మూసి వుంచిన/ సంవృత ఆవరణలో, తక్కువ గాలి అందుబాటు ఉన్న ప్రదేశాలలో స్టవ్ వెలుగుతున్నప్పుడు, లేదా అంతర్గత దహన యంత్రాలు పనిచేయునపుడు కార్బన్ మొనాక్సైడ్ అధిక ప్రమాణంలో ఉత్పత్తి అగును. కార్బన్ మొనాక్సైడ్ను ఆక్సిజన్ సమక్షంలోలేదా వాతావరణం లోని గాలిలో నీలి జ్వాల వెలువరిస్తూ మండి కార్బన్ డయాక్సైడ్ను వెలువరించును.
1960కు ముందు కాలంలో ఇళ్ళలో దీపాలను వెలిగించుటకు, వంట వండుటకు,, వేడి చెయ్యుటకు ఉపయోగించిన కోల్ గ్యాస్, అధిక శాతం కార్బన్ మొనాక్సైడ్ను కలిగి యుండెడిది. ప్రస్తుత ఆధునిక కాలంలో ఇనుప ఖనిజాన్ని కరిగించి ఇనుమును ఉత్పత్తి చెయ్యునపుడు కార్బన్ మొనాక్సైడ్ ఉపఉత్పత్తిగా ఏర్పడు చున్నది.
స్వాభావిక లభ్యత
మార్చుకార్బన్ మొనాక్సైడ్ ప్రకృతిలోని వాతావరణ క్రింది తలంలో (ట్రోపోస్పెయర్) పోటో కెమికల్/కాంతి రసాయన చర్య ఫలితంగా సంవత్సరానికి 5×1012 కిలోగ్రాములు ఉత్పత్తి అగుచున్నది.[4].కార్బన్ మొనాక్సైడ్ లభించు మరికొన్ని సహజ వనరులు అగ్ని పర్వతాలు, అడవులలోని కార్చిచ్చు,, కార్బన్ కలిగిన పదార్థాలు అసంపూర్ణముగా మండటం వలన ఏర్పడు వాయువులు.
చరిత్ర
మార్చుఆరిస్టాటిల్ (384–322 BC) మొదటగా కార్బన్ మొనాక్సైడ్ వాయువు ఉనికి గురించి నమోదు చేసాడు.రాకాసి బొగ్గును (coal) మండించి నపుడు కొన్నివిషవాయులువెలువడుతున్నాయిఅని గుర్తించాడు. 1776 లో ఫ్రెంచి రసాయన శాస్త్రవేత్త డిలాస్సోనే (de Lassone, జింకు ఆక్సైడ్ను కోక్ తో మండించి కార్బన్ మొనాక్సైడ్ను ఉత్పత్తి చేసాడు. అయితే ఈ వాయువు నీలి మంటతో మండటం వలన, హైడ్రోజన్ వాయువు వలన కార్బన్ మొనాక్సైడ్ ఉత్పన్న మగుచున్నదని భావించాడు. 1800 లోస్కాటిష్ శాస్త్రవేత్త William Cumberland Cruikshank కార్బన్ మొనాక్సైడ్ వాయువు, కార్బన్, ఆక్సిజన్ కలిగి ఉన్నదని నిరూపించాడు [5][6].1846లో క్లాడ్ బెర్నాడ్ అనునతడు దీనిని కుక్కలపై పలు మార్లు ప్రయోగించి ఈవాయువు యొక్క విషప్రభావాన్ని నిర్దారణ చేశారు.[7]
రెండవ ప్రపంచ యుద్ధసమయంలో, గ్యాసోలిన్,, డీసెల్ కొరత ఏర్పడిన సమయంలో యంత్ర వాహనాలను నడుపుటకై వాడు వాయు ఇంధన మిశ్రమంలో కార్బన్ మొనాక్సైడ్ను కూడా మిశ్రమం చేసి ఉపయోగించారు.
భౌతిక లక్షణాలు
మార్చుకార్బన్ మొనాక్సైడ్ రంగు, వాసన, రుచి లేనటువంటి, గాలికన్న బరువైన వాయువు.కార్బన్ మొనాక్సైడ్ యొక్క అణుభారం 28.01 గ్రాములు/మోల్. కార్బన్ మొనాక్సైడ్ ద్రవంగా ఉన్నప్పుడు సాంద్రత .789గ్రాములు/సెం.మీ3. కార్బన్ మొనాక్సైడ్ వాయురూపంలో ఉన్నప్పుడు, 0°Cవద్ద, ఒక అట్మాస్ఫియర్ వత్తిడివద్ద కార్బన్ మొనాక్సైడ్ సాంద్రత 1.250 కిలోలు/మీటరు3, 25 °C, ఒక అట్మాస్ఫియర్ (1atm) వత్తిడి వద్ద 1.145 కిలోలు.మీ3సాంద్రత కల్గి ఉండును.కార్బన్ మొనాక్సైడ్ యొక్క ద్రవీభవన స్థానం −205.02 °C (−337.04 °F; 68.13K) ., కార్బన్ మొనాక్సైడ్ యొక్క బాష్పీభవన స్థానం−191.5 °C (−312.7 °F; 81.6K) . 25°Cవద్ద, నీటిలో కార్బన్ మొనాక్సైడ్ యొక్క ద్రావణియత 27.6 మి.గ్రాములు/లీటరుకు.కార్బన్ మొనాక్సైడ్ క్లోరోఫారం, ఎసిటిక్ ఆమ్లం, ఇథైల్ అసిటేట్, ఇథనాల్, అమ్మోనియం హైడ్రాక్సైడ్,, బెంజీన్ లలో కరుగును. మొనాక్సైడ్ యొక్క వక్రీభవన సూచిక 1.0003364.ఈ వాయువు యొక్క ఫ్లాష్ స్థానం −191 °C (−311.8 °F; 82.1K,, కార్బన్ మొనాక్సైడ్ యొక్క తనకు తానుగా మండే/స్వయందహన ఉష్ణోగ్రత (Autoignition temperatute) 609 °C (1, 128 °F; 882K) . ఈ వాయువు యొక్క విశిష్ట ఉష్ణ సామర్ధ్యం 29.1 జౌల్/K మోల్.
అణు లక్షణాలు
మార్చుకార్బన్ మొనాక్సైడ్ యొక్క అణుభారం 28.0.గాలి యొక్క సరాసరి అణుభారం 28.8 .కావున కార్బన్ మొనాక్సైడ్ యొక్క అణుభారం గాలి కన్న కాస్త తక్కువ. కార్బన్, ఆక్సిజన్ పరమాణుల మధ్య బంధ దూరం 112.8 pm.[8] కార్బన్ మొనాక్సైడ్ మూడు కోవాలెంట్/సమయోజనీయ బంధాలు కలిగి ఉండటం వలన, దీని బంధ దూరం నత్రజని (N2) వలె స్థిరమైనది. నత్రజని యొక్క బంధ దూరం, అణుభారం, కార్బన్ మొనాక్సైడ్ కు సమానం.
బంధం-ద్విద్రువ చలనం
మార్చుకార్బన్ మొనాక్సైడ్ అణువులోని కార్బన్, ఆక్సిజన్ పరమాణువులు మొత్తం 10 వేలన్సీ ఎలక్ట్రాను లను కలిగి ఉండును. సామాన్యంగా ఆర్గానిక్ కార్బోనైల్ సమ్మేళనాలలో ఉండు ద్విబందానికి భిన్నంగా, కార్బన్ మొనాక్సైడ్లో కార్బన్ యొక్క అక్టేట్ నియమానుసారంగా, అణువులోని రెండు పరమాణువులు, మూడు బంధిత అణుఆర్బిటాల్ లోని ఆరు వాటాతోకూడిన/ ఉమ్మడివైన ఎలక్ట్రానుల (shared electrons) తో త్రిబందాన్నిఏర్పరచు కున్నది. ఆరు షేర్డ్ /వాటా తోకూడిన/ ఉమ్మడివైన ఎలక్ట్రానులలో, నాలుగు ఎలక్ట్రానులు ఆక్సిజన్ నుండి, మిగిలిన రెండు ఎలక్ట్రానులు కార్బన్ పరమాణువు నుండి నుండిపంచు కోవడం/షేర్ చేసుకోవడం జరిగింది. ఈ మూడు బంధాలలో, ఒక బంధఆర్బిటాల్ ఆక్సిజన్ యొక్క రెండు ఎలక్ట్రాన్లతో నింపబడి, ద్విధ్రువత్వాన్ని (dipolar) చూపును.
దీని వలన మొనాక్సైడ్ అణువులో C ← O మధ్య ధ్రువీకరణము / పోలరైజేషన్ (polarization) వలన, అల్ప స్థాయిలో కార్బన్ పరమాణు మీద ఋణావేశం, ఆక్సిజన్ పరమాణువు మీద స్వల్ప స్థాయిలో ధనావేశం ఏర్పడును. కార్బన్ మొనాక్సైడ్ లోని మిగతా రెండు బంధ కక్ష /ఆర్బిటాల్లో, ప్రతి ఆర్బిటాల్ ఒక ఎలక్ట్రాన్ను ఆక్సిజన్ నుండి, మరో ఎలక్ట్రాన్ను కార్బన్ నుండి కలిగి, ధ్రువీయసమయోజనీయ బంధాన్ని ఏర్పరచుకొని, కార్బన్ పరమాణు కన్న ఆక్సిజన్ పరమాణువు ఎక్కువ ఎలక్ట్రో నెగటివ్ కావున, కార్బన్-ఆక్సిజన్ మధ్య విరుద్ధ ధ్రువీకరణము/రివర్స్ పోలరైజేషన్ (C → O) ఏర్పడి ఉండును. స్వేచ్ఛా కార్బన్ మొనాక్సైడ్ యొక్క అంతిమ ఋణా త్మకత δ-, కార్బన్ వైపు ఉండుటచే, అణువు ద్విధ్రువ చలనం 0.122 D.కలిగి ఉంది.
అందువలన కార్బన్ మొనాక్సైడ్ అణువు అసౌష్టవముగా ఏర్పడి ఉంది. ఆక్సిజన్ ఎలక్ట్రాన్, కార్బన్ కన్న ఎక్కువ సాంద్రత కలిగి, కార్బన్ ఋణాత్మత కన్న ఆక్సిజన్ ఎలక్ట్రాన్ ఎక్కువ ధనాత్మకత కలిగి ఉంది.
బంధ ధ్రువత్వము , ఆక్సీకరణ స్థాయి
మార్చుసిద్ధాంతపరమైన, ప్రయోగ్యాత్మక ఆధ్యయనంలో ఆక్సిజన్ ఎక్కువ ఎలక్ట్రో ఋణాత్మక కలిగినప్పటికీ, కార్బన్ మొనాక్సైడ్ యొక్క ద్విధ్రువచలనదిశ అధిక కార్బన్ ఋణాత్మక నుండి అధిక ధనాత్మక ఆక్సిజన్ వైపు ఉన్నది[9][10] .కార్బన్ మొనాక్సైడ్ లోని మూడు బంధాలు ధ్రువీయ సమయోజనీయ బంధాలు (polar covalent bonds), బలీయంగా ధ్రువికరణ చెంది ఉన్నాయి.కార్బన్ మొనాక్సైడ్ లోని కార్బన్ యొక్క ఆక్సీకరణ స్థాయి +2.
రక్తంలో కార్బన్ మొనాక్సైడ్
మార్చుకార్బన్ మొనాక్సైడ్ను శ్వాసించినప్పుడు, శ్వాస వ్యవస్థ లోని శ్వాస కోశంలో వాయు మార్పిడి వలన కార్బన్ మొనాక్సైడ్ రక్త ప్రవాహంలో చేరును. దేహ వ్యవస్థలో కూడా కార్బన్ మొనాక్సైడ్ హిమగ్లోబిన్ జీవ క్రియలో ఉత్పన్నమై, కణజాలాల ( tissues) ద్వారా రక్తంలో ప్రవేశించును.అందువలన శ్వాస ద్వారా కాకుండా కుడా జీవ కణాలలో కార్బన్ మొనాక్సైడ్ ఉంటుంది.
పారిశ్రామికం గా ఉత్పత్తి
మార్చుపారిశ్రామిక స్థాయిలో కార్బన్ మొనాక్సైడ్ను ఉత్పత్తి చెయ్యుటకు మూల వనరు ప్రొడ్యుసర్ గ్యాస్. అధిక మొత్తంలో కార్బన్ మొనాక్సైడ్, నైట్రోజన్ కలిగిన వాయు మిశ్రమమే ప్రొడ్యుసర్ గ్యాస్. అధిక ఉష్ణోగ్రత వద్ద తక్కువ గాలిలో ఎక్కువ ప్రమాణంలో కార్బన్ను దహించడం వలన ప్రొడ్యుసర్ గ్యాస్ ఏర్పడును. అధిక ఉష్ణోగ్రతలో పొయ్యి/ఒవెన్ లోవత్తుగా పరచబడిన కోక్ (coke) మీదుగా గాలిని ప్రసరింప చేసి ప్రొడ్యుసర్ గ్యాస్ ఉత్పత్తి చెయ్యుదురు. దహనంలో మొదట దశలో ఏర్పడిన కార్బన్ డయాక్సైడ్ వాయువు, తదుపరిఅధిక మొత్తంలో ఉన్న కార్బన్తో తరువాత సమతుల్యత పొందటం వలన కార్బన్ మొనాక్సైడ్ ఏర్పడును. కార్బన్ డయాక్సైడ్ నుండి కార్బన్ మొనాక్సైడ్ ను ఏర్పరచు ఈ ప్రక్రియను బౌడౌర్డ్ రియాక్షన్ (Boudouard reaction) అంటారు.ఈ ప్రక్రియలో 800 °C వద్ద కార్బం మొనాక్సైడ్ ఉత్పత్తి అగును.
- CO2 + C → 2CO (ΔH = 170 కిలో జౌల్/మోల్)
వాటర్ గ్యాస్ నుండి కూడా కార్బన్ మొనాక్సైడ్ వాయువును ఉత్పత్తి చే య్యుదురు. ఆవిరి, కార్బన్ లమధ్య ఉష్ణ గ్రాహాక (endothermic) చర్య వలన కార్బన్ మొనాక్సైడ్, హైడ్రోజన్ వాయువుల మిశ్రమం ఉత్పత్తి అగును .
- H2O + C → H2 + CO (ΔH = +131 కిలో జౌల్/మోల్)
మరో ప్రక్రియ ఉత్పత్తి విధానంలో, సహజ వాయువునుండి వాయువులను సంశ్లేషణచెయ్యడం వలన కూడా కార్బన్ మొనాక్సైడ్ ఉత్పత్తి అగును.మరొక విధానంలో లోహ ఖనిజ ఆక్సైడ్ లను క్షయికరించునపుడు కార్బన్ మొనాక్సైడ్ ఉప ఉత్పత్తి ఏర్పడును.
- MO + C → M + CO
మితంగా ఆక్సిజన్ లేదా గాలిని కార్బన్ కుఅందుబాటులో ఉంచి నేరుగా కార్బన్ ను ఆక్సీకరణ చెయ్యడం వలన కూడా కార్బన్ మొనాక్సైడ్ను ఉత్పత్తి చెయ్యుదురు .
- 2C(s) + O2 → 2CO(g)
ప్రయోగ/పరిశోధనశాలలో ఉత్పత్తి
మార్చుప్రయోగశాలలో కార్బన్ మొనాక్సైడ్ను రెండు మూడు విధానాలలో ఉత్పత్తి కావించెదరు. ఒక పద్ధతిలో ఫార్మిక్ ఆసిడ్ లేదా ఆక్సాలిక్ ఆమ్లాన్ని, గాఢ సల్ఫ్యూరిక్ ఆమ్లం వంటి దానితో నిర్జలీకరణ (dehydration ) కావించుట ద్వారా ఉత్పత్తి చెయ్యుదురు.మరొక పద్ధతిలో పొడిగా చెయ్యబడిన జింకు లోహం, కాల్షియం కార్బోనేట్ మిశ్రమాన్ని బాగా వేడి చెయ్యడం వలన కూడా ఉత్పత్తి కావించెదరు.
- Zn + CaCO3 → ZnO + CaO + CO
అయోడో ఫార్మ్, సిల్వర్ నైట్రేట్ మిశ్రమం నుండి కూడా కార్బన్ మొనాక్సైడ్ ఉత్పత్తి చెయ్యవచ్చును.
- CHI3 + 3AgNO3 + H2O → 3HNO3 + CO + 3AgI
చాలా లోహాలు, కార్బన్ మొనాక్సైడ్ తో సహజసంయోజక బంధం కలిగిన సమన్వయంసంక్లిష్ట పదార్థాలను (complexes ) ఏర్పరుచును. అయితే తక్కువ ఆక్సీకరణస్థాయిగల లోహాలుమాత్రమే కార్బన్ మొనాక్సైడ్ లింగడ్స్ (ligands) లతో సంక్లిష్టసంయోగ పదార్థాలను ఏర్పరచును.నికెల్ లోహం నేరుగా కార్బన్ మొనాక్సైడ్తో సంయోగం వలన నికెల్ కార్బోనైల్ ఏర్పడును.
- Ni + 4 CO → Ni(CO)4 (1 bar,55°C)
నికెల్ కార్బోనైల్, ఇతర కార్బోనైల్లలో కార్బన్మీది ఎలక్ట్రాన్జంట లోహంతో ప్రతిస్పందించుతుంది. కార్బన్ మొనాక్సైడ్ ఎలక్ట్రాన్ జంటను, లోహానికిఅర్పించును/ దానమిచ్చును. ఇక్కడ, ఈచర్యలో కార్బన్ మొనాక్సైడ్ కార్బోనైల్ లిగండ్ (carbonyl ligand) గా పిలువ బడుచున్నది.కార్బోనైల్లలో ముఖ్యమైన లోహ కార్బోనైల్ ఐరన్ పెంటా కార్బోనైల్ (Fe (CO) 5.
చాలా లోహ-కార్బన్ మొనాక్సైడ్ సంక్లిష్ట పదార్థాలు, కార్బన్ మొనాక్సైడ్ నుండి కాకుండా, ఆర్గానిక్ ద్రావణుల డికార్బనైలేసన్ (decarbonylation) వలన ఏర్పడును. ఉదాహరణకు iridium trichloride, triphenylphosphine లు మరుగుచున్న 2-2-methoxyethanol లేదాDMF తో చర్య వలన IrCl (CO) (PPh3) 2 ఏర్పడును.
రసాయన చర్యలు
మార్చుబలమైన ఆమ్లాలు, నీటి సమక్షములో కార్బన్ మొనాక్సైడ్ ఆల్కిన్స్తో చర్యజరిపి కార్బోక్సిలిక్ ఆమ్లాలను ఏర్పరచును. ఈ రసాయన చర్యను కోచ్-హాఫ్ రసాయన (Koch–Haaf reaction) చర్య అంటారు.గట్టర్ మాన్-కోచ్ ( Gattermann–Koch reaction) రసాయనచర్యలో అల్యూమినియం క్లోరైడ్ (AlCl3) లేదా హైడ్రోక్లోరిక్ ఆమ్లం (HCl) ల సమక్షంలో అరెనెస్ (arenes, బెంజాల్ డిహైడ్ దేరివేట్లు ఉత్పన్నమగును.ఆర్గాన్ లిథియం సమ్మేళనాలు కార్బన్ మొనాక్సైడ్తో రసాయన చర్య జరుపును, కాని వీటి ఉత్పత్తులవలన శాస్త్రపరమైన ఉపయోగం పెద్దగా లేదు.
కార్బోకేటాయాన్స్, కార్బోఅయాన్లతో కార్బన్ మొనాక్సైడ్ చర్యాశీలత కలిగిఉన్నప్పటికీ, లోహ ఉత్పేరకం ప్రమేయం లేనిచో ఆర్గానిక్ సమ్మేళనాలతో కార్బన్ మొనాక్సైడ్ చర్యారహితం. 5 గిగా పాస్కల్ కన్నఎక్కువ వత్తిడివద్ద కార్బన్ మొనాక్సైడ్, కార్బన్, ఆక్సిజన్ల ఘన పాలిమర్గా పరివర్తన చెందును. ఇది వాతావరణ వత్తిడి వద్ద మెటా స్టేబుల్ అయినప్పటికీ, శక్తి వంతమైన ప్రేలుడు పదార్థంగా ప్రవర్తించును.
విష ప్రభావం
మార్చుపలు దేశాలలో కార్బన్ మొనాక్సైడ్ వలన జరుగు ప్రాణాంతకమైన గాలి కాలుష్యం సాధారణం.[11] కార్బన్ మొనాక్సైడ్ రంగు, వాసన, రుచి లేని వాయువు అయినప్పటికీ, అత్యంత ప్రాణి హాని కల్గించు విష వాయువు.కార్బన్ మొనాక్సైడ్ రక్తంలోని హీమోగ్లోబిన్తో కలవడం వలన కార్బోక్సిహీమోగ్లోబిన్ ఉత్పత్తి అగును. రక్తంలోని హీమోగ్లోబిన్ దేహ కణజాలానికి ఆక్సిజన్ను సరఫరా చేస్తుంది. రక్తంలోని హీమోగ్లోబిన్తో పాటు కార్బోక్సిహీమోగ్లోబిన్ ఉండటం వలన, ఆక్సిజన్ను కణజాలానికి అందించు హీమోగ్లోబిన్ సామర్ధ్యం గణనీయంగా తగ్గిపోతుంది. రక్తంలో కార్బన్ మొనాక్సైడ్ 667 ppm ప్రమాణంలో ఉన్నచో, 50% హీమోగ్లోబిన్ను కార్బోక్సి హీమోగ్లోబిన్గా పరివర్తించును.రక్తంలోని హిమోగ్లోబిన్లో 50 % వరకు కార్బోక్సి హీమోగ్లోబిన్ ఉన్నచో కోమాలోకి వెళ్ళడం లేదా మరణించడం జరుగుతుంది.
కార్బన్ మొనాక్సైడ్ విషప్రభావానికి గురైనప్పుడు తలనొప్పిగాఉండటం, వాంతి అవుతున్నట్లు ఉండటం, వాంతులు రావడం, తలతిప్పట, కళ్ళు తిరగటం, ఆయాసం, చికాకుగా ఉండటం, బలహీన పడటం వంటి లక్షణాలు కన్పిస్తాయి. ఇలాంటి లక్షణాలను కొన్ని సార్లు విషాహార సేవనం వలన అని పొరపాటు పడుతుంటారు. చిన్న పిల్లలు కార్బన్ మొనాక్సైడ్ ప్రభావానికి గురైనప్పుడు ఆహారం తినకపోవడం, చికాకు పడటం చేస్తారు.నరాలకు/నాడిమండలానికి సంబంధించి తికమకపడటం, అయోమయంగా అన్పించడం, దృష్టి పరమైన ఇబ్బందులు ఏర్పడం, సృహ తప్పడం, వంటివి జరుగును.
కార్బన్ మొనాక్సైడ్ దేహ వ్యవస్థలోని మైయో గ్లోబిన్, మైటోకాండ్రియాల్ సైటోక్రోమ్ ఆక్సిడేస్ (mitochondrial cytochrome oxidase) లతో కుడా కలిసి పోతుంది. ఫలితంగా గుండెకు, కేంద్రనాడీవ్యవస్థకు నష్టం కలిగించును. కార్బన్ మొనాక్సైడ్ గర్భిణీ స్త్రీలయొక్క కడుపులోని పిండంపై దుష్ఫలితాలు కల్గించును.
సూక్ష్మజీవ శాస్త్రం/విజ్ఞానం
మార్చుమెథానోజేనిక్ ఆర్చే యొక్క పోషక పదార్థం లేక ఆహారం కార్బన్ మొనాక్సైడ్. మెథానోజేనిక్ ఆర్చే అనునది అసెటైల్ కొఎంజైం A యొక్క నిర్మాణానికి మూలఆధారం.బాక్టీరియాలలో కార్బన్ మొనాక్సైడ్ డిహైడ్రోజెనేస్ అను ఎంజైమ్ కార్బన్ డయాక్సైడ్ని క్షయికరించడం వలన కార్బన్ మొనాక్సైడ్ ఏర్పడును.
CooA అనునది కార్బన్ మొనాక్సైడ్ యొక్క సెన్సర్ ప్రోటీన్.అయితే జీవ వ్యవస్థలో దీని పాత్ర, ప్రభావం గురించి ఎటువంటి సమాచారం లభించలేదు.
వాతవరణంలో కార్బన్ మొనాక్సైడ్ ఉనికి
మార్చుకార్బన్ మొనాక్సైడ్ వాతావరణంలో స్వాభావికంగాను, కల్పిత వాతావరణం పరిసరాల్లో, వివిధ గాఢతలలో ఉంది.దిగువన పట్టికలో వివిధ పరిసరాలలో ఉండు కార్బన్ మొనాక్సైడ్ గాఢతలను ఇవ్వడం జరిగింది.
| వాయువు గాఢత | పరిసరాల వివరాలు |
| 0.1 ppmv | స్వాభావిక పరిసర పరిస్థితిలో ఉండు గాఢ త |
| 0.5–5 ppmv | ఇళ్ళలో ఉండు సరాసరి స్థాయి. |
| 5–15 ppmv | అదునాతమైన వాహనాలనుంది, స్టవ్ లనుండి వెలువడు స్థాయి |
| 17 ppmv | శుక్ర గ్రహం మీదివాతావరణం |
| 700 ppmv | అంగారక గ్రహం మీది వాతావరణము |
| 5, 000 ppmv | ఇళ్ళలో కలపను మండించడం వలన ఏర్పడు స్థాయి. |
| 7, 000 ppmv | కాటలిక్ కన్వర్టరు లేని కారునుం ది వెలువడు వాయు స్థాయి. |
- సూచన:ppmv అనగా parts per million,volume(ఘనపరిమాణం ప్రకారం పదిలక్షలవంతులో ఒకవంతు)
ఉపయోగాలు
మార్చురసాయన పరిశ్రమలలో వినియోగం
మార్చుపలు రసాయనాలను వాణిజ్య పరంగా భారి ప్రమాణంలో ఉత్పత్తి చెయ్యుటకై కార్బన్ మొనాక్సైడ్ను పరిశ్రమలలో ఉపయోగిస్తారు.[12] అల్కేన్స్ .కార్బన్ మొనాక్సైడ్,, హైడ్రోజన్ల హైడ్రోఫర్మైలేసన్ (hydroformylation) చర్య ద్వారా అధిక ప్రమాణంలో అల్దిహైడులను ఉత్పత్తిచెయ్యుదురు.షెల్ హైయర్ ఒలేఫిన్ (Shell Higher Olefin ) ప్రక్రియతో కూడిన హైడ్రోఫర్మలేసన్ విధానం, డేటెర్జెంట్ ల ఉత్పత్తికి పుర్వగామి ప్రక్రియ.
ఐసో సైనేట్స్, పాలికార్బోనేట్స్,, పాలియురేతేన్స్లను ఉత్పత్తి చెయ్యుటకై ఉపయోగించు ఫొస్జెన్ (Phosgene) ను కార్బన్ మొనాక్సైడ్ నుండి ఉత్పత్తి చేయ్యుదురు. పోరస్ ఆక్టివేటేడ్ కార్బన్ పదార్థం (ఉత్ప్రేరకంగా పనిచేయును) మీదుగా శుద్ధి కావించబడిన కార్బన్ మొనాక్సైడ్, క్లోరిన్ వాయువులను ప్రసరింప చెయ్యడం, పంపడం ద్వారా ఫొస్జెన్ (Phosgene) వాయువును ఉత్పత్తి చెయ్యుదురు.
- CO + Cl2 → COCl2
కార్బన్ మొనాక్సైడ్ను ఉదజనీకరణం (hydrogenation ) చెయ్యడం ద్వారా మెథనాల్ను తయారు చేయుదురు.ఈ ఉదజనీకరణ ప్రక్రియలో కార్బన్ మొనాక్సైడ్, కార్బన్-కార్బన్ బంధంతో జతగుడటం వలన మెథనాల్ ఏర్పడును.ఫిసర్ –ట్రోప్ష్ (Fischer-Tropsch) విధానంలో కార్బన్ మొనాక్సైడ్ ఉదజనీకరణ వలన ద్రవ హైడ్రోకార్బన్ ఇంధనం ఏర్పడును. ఈ సాంకేతికవిజ్ఞానము ద్వారా బొగ్గు లేదా జీవపదార్థాన్ని డీసెల్ గా పరివర్తించ వచ్చును.
మొన్సంటో ప్రక్రియ పద్ధతిలో రోడియం ఉత్పేరకం, హైడ్రో ఐయోడిక్ ఆమ్లంల సమక్షంలో కార్బన్ మొనాక్సైడ్, మెథనాల్ల చర్యవలన అసిటిక్ ఆమ్లం ఏర్పడును. ఈ ఉత్పత్తి విధానంలో అధిక మొత్తంలో పరిశ్రమ స్థాయిలో అసిటిక్ ఆమ్లాన్ని ఉత్పత్తి చేస్తున్నారు.
మొండ్ ప్రక్రియలో (Mond process) లో నికెల్ లోహాన్ని శుధ్ధి చెయ్యుటకు కార్బన్ మొనాక్సైడ్ ను ఉపయోగిస్తారు.
లేసరులలో
మార్చుఅధిక శక్తి వంతమైన పరారుణ కిరణలేసరులలో కార్బన్ మొనాక్సైడ్ను ఉపయోగిస్తారు
ఇతర వినియోగాలు
మార్చుఅంగార గ్రహం మీద ఇంధనంగా వాడుటకు ప్రతిపాందించారు. అంగార గ్రహం మీద ఉపరితల రవాణకై కార్బన్ మొనాక్సైడ్ /ఆక్సిజన్ ఇంధన యంత్రాలను సిఫారసు చేసారు. అంగార గ్రహం మీది వాతావరణం నుండి జిర్కొనియ విద్యుద్విశ్లేషణ విధానంలో, మార్టియన్ నీటి వనరులను ఉపయోగించకయే హైడ్రోజన్ వాయువును ఉత్పత్తి చెయ్య వచ్చును. ఉత్పన్నమైన హైడ్రోజన్ నుండి మిథేన్, హైడ్రోజన్ ఆధారిత ఇంధనాలను ఉత్పన్నం చెయ్యవచ్చును.
ఇవికూడా చూడండి
మార్చుమూలాలు
మార్చు- ↑ 1.0 1.1 "Carbon monoxide". Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ↑ NIOSH Pocket Guide to Chemical Hazards. "#0105". National Institute for Occupational Safety and Health (NIOSH).
- ↑ http://cameochemicals.noaa.gov/chemical/335
- ↑ Weinstock, B.; Niki, H. (1972). "Carbon Monoxide Balance in Nature". Science. 176 (4032): 290–2. Bibcode:1972Sci...176..290W. doi:10.1126/science.176.4032.290. PMID 5019781.
- ↑ Cruickshank, W. (1801) "Some observations on different hydrocarbonates and combinations of carbone with oxygen, etc. in reply to some of Dr. Priestley's late objections to the new system of chemistry," Journal of Natural Philosophy, Chemistry and the Arts [a.k.a. Nicholson's Journal], 1st series, 5 : 1–9.
- ↑ Cruickshank, W. (1801) "Some additional observations on hydrocarbonates, and the gaseous oxide of carbon," Journal of Natural Philosophy, Chemistry and the Arts, 1st series, 5 : 201–211.
- ↑ Waring, Rosemary H.; Steventon, Glyn B.; Mitchell, Steve C. (2007). Molecules of death. Imperial College Press. p. 38. ISBN 1-86094-814-6.
- ↑ Gilliam, O. R.; Johnson, C. M.; Gordy, W. (1950). "Microwave Spectroscopy in the Region from Two to Three Millimeters". Physical Review. 78 (2): 140–144. Bibcode:1950PhRv...78..140G. doi:10.1103/PhysRev.78.140.
- ↑ Blanco, Fernando; Alkorta, Ibon; Solimannejad, Mohammad; Elguero, Jose (2009). "Theoretical Study of the 1:1 Complexes between Carbon Monoxide and Hypohalous Acids". J. Phys. Chem. A. 113 (13): 3237–3244. doi:10.1021/jp810462h. PMID 19275137.
- ↑ Meerts, W; De Leeuw, F.H.; Dymanus, A. (1 June 1977). "Electric and magnetic properties of carbon monoxide by molecular-beam electric-resonance spectroscopy". Chemical Physics. 22 (2): 319–324. Bibcode:1977CP.....22..319M. doi:10.1016/0301-0104(77)87016-X.
- ↑ Omaye ST (2002). "Metabolic modulation of carbon monoxide toxicity". Toxicology. 180 (2): 139–150. doi:10.1016/S0300-483X(02)00387-6. PMID 12324190.
- ↑ Elschenbroich, C.; Salzer, A. (2006). Organometallics: A Concise Introduction (2nd ed.). Weinheim: Wiley-VCH. ISBN 3-527-28165-7.

