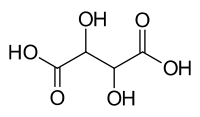
టార్టారిక్ ఆమ్లం
టార్టారిక్ ఆమ్లం తెలుపు, స్ఫటికాకారంలో గల సేంద్రియ ఆమ్లం. ఇది చాలా పండ్లలో సహజంగా లభ్యమవుతుంది. ముఖ్యంగా ద్రాక్షలో ఉంటుంది. కానీ అరటి, చింతపండు, సిట్రస్ జాతి పండ్లలో కూడా ఉంటుంది. [4] దీని లవణం, పొటాషియం బిటార్ట్రేట్, సాధారణంగా క్రీమ్ ఆఫ్ టార్టార్ గా పిలుస్తారు. ఇది వైన్ తయారీ ప్రక్రియలో ఉపయోగ పడుతుంది. దీనిని సాధారణంగా సోడియం బైకార్బోనేట్తో కలుపుతారు. దీనిని ఆహార తయారీలో పులియబెట్టే కారకంగా ఉపయోగించే బేకింగ్ పౌడర్గా అమ్ముతారు. ఆమ్లం యాంటీఆక్సిడెంట్ E334 గా ఆహారాలలో కలుపబడుతుంది. ఇది విలక్షణమైన పుల్లని రుచిని కలిగి ఉంటుంది. టార్టారిక్ ఆమ్లం ఆల్ఫా-హైడ్రాక్సీ- కార్బాక్సిలిక్ ఆమ్లం. ఇది ఆమ్ల లక్షణాలతో డైప్రోటిక్, ఆల్డారిక్ గా ఉంటుంది. ఇది సక్సినిక్ ఆమ్లానికి డైహైడ్రాక్సిల్ ఉత్పన్నం.
| |

| |
| పేర్లు | |
|---|---|
| Preferred IUPAC name
2,3-Dihydroxybutanedioic acid | |
| ఇతర పేర్లు
Tartaric acid
2,3-Dihydroxysuccinic acid Threaric acid Racemic acid Uvic acid Paratartaric acid Winestone | |
| గుర్తింపు విషయాలు | |
| సి.ఎ.ఎస్. సంఖ్య | [526-83-0] |
| పబ్ కెమ్ | 875 |
| డ్రగ్ బ్యాంకు | DB01694 |
| కెగ్ | C00898 |
| వైద్య విషయ శీర్షిక | tartaric+acid |
| సి.హెచ్.ఇ.బి.ఐ | CHEBI:15674 |
| SMILES | O=C(O)C(O)C(O)C(=O)O |
| |
| ధర్మములు | |
| C4H6O6 (Basic formula) HO2CCH(OH)CH(OH)CO2H (Structural formula) | |
| మోలార్ ద్రవ్యరాశి | 150.087 g/mol |
| స్వరూపం | White powder |
| సాంద్రత | 1.79 g/mL (H2O) |
| ద్రవీభవన స్థానం | 171 నుండి 174 °C (340 నుండి 345 °F; 444 నుండి 447 K) (L or D-tartaric; pure) 206 °C (DL, racemic) 165–166 °C (meso-anhydrous) 146–148 °C (meso-hydrous)[3] |
| |
| ఆమ్లత్వం (pKa) | L(+) 25 °C : pKa1= 2.89, pKa2= 4.40 meso 25 °C: pKa1= 3.22, pKa2= 4.85 |
| అయస్కాంత ససెప్టిబిలిటి | −67.5·10−6 cm3/mol |
| ప్రమాదాలు | |
| ఇ.యు.వర్గీకరణ | {{{value}}} |
| R-పదబంధాలు | R36 |
| సంబంధిత సమ్మేళనాలు | |
ఇతర కాటయాన్లు
|
Monosodium tartrate Disodium tartrate Monopotassium tartrate Dipotassium tartrate |
| Related {{{label}}} | {{{value}}} |
సంబంధిత సమ్మేళనాలు
|
2,3-Butanediol Cichoric acid |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |
| Infobox references | |
చరిత్ర
మార్చుటార్టారిక్ ఆమ్లం వైన్ తయారీదారులకు శతాబ్దాలుగా తెలుసు. వైన్ తయారీ అవక్షేపాల నుండి దాని వెలికితీతకు సంబంధించిన లిఖితపూర్వక రికార్డు, సిర్కా 800 AD లో రసవాది అయిన జాబిర్ ఐబిన్ హాయన్ పేర్కొన్నాడు. [5] దీని నిష్కర్షణ కోసం రసాయన ప్రక్రియను 1769 లో స్వీడిష్ రసాయన శాస్త్రవేత్త కార్ల్ విల్హెల్మ్ షీలే అభివృద్ధి చేశాడు. [6]
రసాయన చిరాలిటీని కనుగొనడంలో టార్టారిక్ ఆమ్లం ముఖ్యమైన పాత్ర పోషించింది. టార్టారిక్ ఆమ్లం ధర్మాలను మొట్టమొదట 1832 లో జీన్ బాప్టిస్ట్ బయోట్ పరిశీలించాడు. అతను ధ్రువణ కాంతిని భ్రమణం చేయించగల సామర్థ్యాన్ని గమనించాడు. [7] [8] లూయిస్ పాశ్చర్ 1847 లో సోడియం అమ్మోనియం టార్ట్రేట్ స్ఫటికాల ఆకృతులను పరిశోధించడం ద్వారా ఈ పరిశోధనను కొనసాగించి, దాని అణువు లేదా అయాన్ ని కనుగొన్నాడు. భిన్నంగా ఆకారంలో ఉన్న స్ఫటికాలను మానవీయంగా క్రమబద్ధీకరించడం ద్వారా, పాస్టెయర్ మొట్టమొదటిసారిగా లెవోటార్టారిక్ ఆమ్లం యొక్క స్వచ్ఛమైన నమూనాను ఉత్పత్తి చేశాడు. [9] [10] [11] [12] [13]
స్టీరియో కెమిస్ట్రి
మార్చుసహజంగా సంభవించే టార్టారిక్ ఆమ్లం అణువు లేదా అయాన్. ఇది సేంద్రీయ రసాయన సంశ్లేషణలో ఉపయోగకరమైన ముడి పదార్థం. సహజంగా లభ్యమయ్యే ఆమ్ల రూపం డెక్స్ట్రో టార్టారిక్ ఆమ్లం లేదా ఎల్ - (+) - టార్టారిక్ ఆమ్లం (వాడుకలో లేని పేరు డి- టార్టారిక్ ఆమ్లం). ఇది సహజంగా లభ్యమవుతున్నందున, ఇది దాని ఎన్యాంటియోమర్ , మీసో ఐసోమర్ కంటే కొంచెం చౌకగా ఉంటుంది. డెక్స్ట్రో, లెవో వంటి పూర్వలగ్నాలు ప్రాచీన పదాలు. [14] ఆధునిక పాఠ్యపుస్తకాలలో సహజ రూపాన్ని (2 R, 3 R ) -టార్టారిక్ ఆమ్లం ( L - (+) - టార్టారిక్ ఆమ్లం) గా, దాని ఎన్యాంటియోమర్ (2 S, 3 S ) -టార్టారిక్ ఆమ్లం ( D - (-) - టార్టారిక్ ఆమ్లం) గా తెలుపుతారు. దాని మెసో డయాస్టీరియోమెర్ (2 R, 3 S) -టార్టారిక్ ఆమ్లం.
రెండు చిరల్ స్టీరియో ఐసోమర్లు తలం ధ్రువణ కాంతిని వ్యతిరేక దిశల్లో భ్రమణం చెందించగా, మీసో-టార్టారిక్ ఆమ్లం ద్రావణాలు తలం -ధ్రువణ కాంతిని భ్రమణం చెందించవు. [15] [16]
| DL -టార్టారిక్ ఆమ్లం ( రేసెమిక్ ఆమ్లం ) (1 : 1 నిష్పత్తిలో ఉన్నప్పుడు) | మెసోటార్టారిక్ ఆమ్లం | |
|---|---|---|
| డెక్స్ట్రోటార్టారిక్ ఆమ్లం |
లెవోటార్టరిక్ ఆమ్లం | |
ఉత్పత్తి
మార్చుటార్టారిక్ ఆమ్లం ఎల్ - (+) - టార్టారిక్ ఆమ్లం ఐసోమర్ పారిశ్రామికంగా అతిపెద్ద మొత్తంలో ఉత్పత్తి అవుతుంది. ఇది కిణ్వ ప్రక్రియలో ఘన ఉప ఉత్పత్తి అయిన లీస్ నుండి పొందబడుతుంది. పూర్వ ఉపఉత్పత్తులు ఎక్కువగా పొటాషియం బిటార్ట్రేట్ (KHC 4 H 4 O 6 ) కలిగి ఉంటాయి. ఈ పొటాషియం ఉప్పును కాల్షియం హైడ్రాక్సైడ్(Ca (OH) 2 ) తో కలిసినపుడు తరువాత కాల్షియం టార్ట్రేట్ (CaC 4 H 4 O 6 ) గా మార్చబడుతుంది: [17]
KO 2 CCH (OH) CH (OH) CO 2 H + Ca (OH) 2 → Ca (O 2 CCH (OH) CH (OH) CO 2 ) + KOH + H 2 O
ఆచరణలో, కాల్షియం క్లోరైడ్ చేరికతో కాల్షియం టార్ట్రేట్ అధిక దిగుబడి లభిస్తుంది. కాల్షియం టార్ట్రేట్ తరువాత లవణంతో సజల సల్ఫ్యూరిక్ ఆమ్లంతో కలపడం ద్వారా టార్టారిక్ ఆమ్లంగా మార్చబడుతుంది:
Ca (O 2 CCH (OH) CH (OH) CO 2 ) + H 2 SO 4 → HO 2 CCH (OH) CH (OH) CO 2 H + CaSO 4
చర్యాశీలత
మార్చుL - (+) - టార్టారిక్ ఆమ్లం, అనేక చర్యలలో పాల్గొనవచ్చు. దిగువ చర్యలో చూపినట్లుగా, ఫెర్రస్ లవణం సమక్షంలో హైడ్రోజన్ పెరాక్సైడ్తో L - (+) - టార్టారిక్ ఆమ్లం చర్య జరపడంతో డైహైడ్రాక్సీమాలిక్ ఆమ్లం ఉత్పత్తి అవుతుంది.
HO 2 CCH (OH) CH (OH) CO 2 H + H 2 O 2 → HO 2 CC (OH) C (OH) CO 2 H + 2 H 2 O
డైహైడ్రాక్సీమాలిక్ ఆమ్లం తరువాత నైట్రిక్ ఆమ్లంతో టార్ట్రానిక్ ఆమ్లానికి ఆక్సీకరణం చెందిస్తుంది. [18]
ఉత్పన్నాలు
మార్చుటార్టారిక్ ఆమ్లం యొక్క ముఖ్యమైన ఉత్పన్నాలు దాని లవణాలు, టార్టార్ క్రీమ్ ( పొటాషియం బిటార్ట్రేట్ ), రోషెల్ ఉప్పు (పొటాషియం సోడియం టార్ట్రేట్, తేలికపాటి విరేచనకారి ), టార్టార్ ఎమెటిక్ (యాంటీమోనీ పొటాషియం టార్ట్రేట్)లు. [19] [20] [21] డైసోప్రొపైల్ టార్ట్రేట్ను అసమాన సంశ్లేషణలో సహ-ఉత్ప్రేరకంగా ఉపయోగిస్తారు.
టార్టారిక్ ఆమ్లం ఒక కండరాల జీవ విషం., ఇది మాలిక్ ఆమ్లం ఉత్పత్తిని నిరోధించడం ద్వారా పనిచేస్తుంది. అధిక మోతాదులో పక్షవాతం, మరణానికి కారణమవుతుంది. [22] మధ్యస్థ ప్రాణాంతక మోతాదు (LD50) మనిషికి 7.5 గ్రాములు / కిలోలు, కుందేళ్ళకు 5.3 గ్రాములు / కిలోలు, ఎలుకలకు 4.4 గ్రాములు / కిలోలు. [23] ఈ సంఖ్యను చూస్తే 70 కి.గ్రా. (150 పౌ.) బరువున్న వ్యక్తిని చంపడానికి ఇది 500 గ్రా. (18 oz) పైగా ఆవసరమవుతుంది. కాబట్టి ఇది చాలా ఆహారాలలో, ముఖ్యంగా పుల్లని రుచిగల స్వీట్లలో సురక్షితంగా చేర్చబడవచ్చు. ఆహార సంకలితంగా, టార్టారిక్ ఆమ్లం E సంఖ్య E334 తో యాంటీఆక్సిడెంట్గా ఉపయోగించబడుతుంది.
టార్టార్ యొక్క క్రీమ్ నీటిలో కలిపినప్పుడు ఏర్పడిన కాంజికాభ ద్రావణం (సస్పెన్షన్) రాగి నాణేలను బాగా శుభ్రం చేయడానికి ఉపయోగపడుతుంది. ఎందుకంటే టార్ట్రేట్ ద్రావణం నాణెం యొక్క ఉపరితలంపై ఉన్న రాగి (II) ఆక్సైడ్ పొరను కరిగించగలదు. ఫలితంగా రాగి (II) -టార్ట్రేట్ కాంప్లెక్స్ నీటిలో సులభంగా కరుగుతుంది.
వైన్లో టార్టారిక్ ఆమ్లం
మార్చుటార్టారిక్ ఆమ్లం వైన్ తాగేవారికి "వైన్ డైమండ్స్" మూలంగా వెంటనే గుర్తించబడవచ్చు. చిన్న పొటాషియం బిటార్ట్రేట్ స్ఫటికాలు కొన్నిసార్లు కార్క్ లేదా బాటిల్ దిగువన ఆకస్మికంగా ఏర్పడతాయి. ఈ "టార్ట్రేట్లు" ప్రమాదకరం కావు. కొన్నిసార్లు వీటిని విరిగిన గాజు అని తప్పుగా భావించినప్పటికీ, కోల్డ్ స్టెబిలైజేషన్ ద్వారా చాలా వైన్లలో నిరోధించబడతాయి.
టార్టారిక్ ఆమ్లం రసాయనికంగా ఒక ముఖ్యమైన పాత్ర పోషిస్తుంది. ఇది కిణ్వ ప్రక్రియలో pH ను అవాంఛనీయమైన చెడిపోయే బ్యాక్టీరియా జీవించలేని స్థాయికి తగ్గించడం , కిణ్వ ప్రక్రియ తర్వాత సంరక్షణకారిగా పనిచేస్తుంది. నోటిలో, టార్టారిక్ ఆమ్లం వైన్లో కొంత టార్టైన్ ను అందిస్తుంది, అయినప్పటికీ సిట్రిక్, మాలిక్ ఆమ్లాలు కూడా వాటి పాత్ర పోషిస్తాయి.
పండ్లలో టార్టారిక్ ఆమ్లం
మార్చుసిట్రస్లో, సేంద్రీయ వ్యవసాయంలో ఉత్పత్తి చేయబడిన పండ్లలో సాంప్రదాయ వ్యవసాయంలో ఉత్పత్తి చేయబడిన పండ్ల కంటే ఎక్కువ స్థాయిలో టార్టారిక్ ఆమ్లం ఉంటుంది. [24]
అనువర్తనాలు
మార్చుటార్టారిక్ ఆమ్లం, దాని ఉత్పన్నాలు ఔషధ రంగంలో చాలా ఉపయోగాలు కలిగి ఉన్నాయి. ఉదాహరణకు, నోటి ఔషధాల రుచిని మెరుగుపరచడానికి సిట్రిక్ యాసిడ్తో కలిపి, లవణాల ఉత్పత్తిలో ఇది ఉపయోగించబడింది. [25]
మూలాలు
మార్చు- ↑ Tartaric Acid – Compound Summary, PubChem.
- ↑ Dawson, R.M.C. et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ↑ Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics (86th ed.). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ↑ Duarte, A.M.; Caixeirinho, D.; Miguel, M.G.; Sustelo, V.; Nunes, C.; Fernandes, M.M.; Marreiros, A. (2012). "ORGANIC ACIDS CONCENTRATION IN CITRUS JUICE FROM CONVENTIONAL VERSUS ORGANIC FARMING". Acta Horticulturae (933): 601–606. doi:10.17660/actahortic.2012.933.78. ISSN 0567-7572. Archived from the original on 2018-06-02. Retrieved 2020-03-25.
- ↑ Lisa Solieri, Paolo Giudici (2009). Vinegars of the World. Springer. p. 29. ISBN 88-470-0865-4.
- ↑ Retzius, Anders Jahan (1770) "Försök med vinsten och dess syra" (Experiments with cream of tartar and its acid), Kungliga Vetenskapsakademiens Handlingar (Proceedings of the Royal Academy of Sciences), 31 : 207–213. From p. 209: "§. 6. Dessa försök omtalte jag för Hr. Carl Wilhelm Scheele (en snabb och lårgirug Pharmaciæ Studiosus) … " (§. 6. I mention these experiments on behalf of Mr. Carl Wilhelm Scheele (a quick and studious student of pharmacology) … )
- ↑ Biot (1835) "Mémoire sur la polarization circulaire et sur ses applications à la chimie organique" (Memoir on circular polarization and on its applications to organic chemistry), Mémoires de l'Académie des sciences de l'Institut, 2nd series, 13 : 39–175. That tartaric acid (acide tartarique cristallisé) rotates plane-polarized light is shown in Table G following p. 168. (Note: This article was read to the French Royal Academy of Sciences on 1832 November 5.)
- ↑ Biot (1838) "Pour discerner les mélanges et les combinaisons chimiques définies ou non définies, qui agissent sur la lumière polarisée; suivies d'applications aux combinaisons de l'acide tartarique avec l'eau, l'alcool et l'esprit de bois" (In order to discern mixtures and chemical combinations, defined or undefined, which act on polarized light; followed by applications to combinations of tartaric acid with water, alcohol [i.e., ethanol], and spirit of wood [i.e., methanol]), Mémoires de l'Académie des sciences de l'Institut, 2nd series, 15 : 93–279.
- ↑ L. Pasteur (1848) "Mémoire sur la relation qui peut exister entre la forme cristalline et la composition chimique, et sur la cause de la polarisation rotatoire" (Memoir on the relationship which can exist between crystalline form and chemical composition, and on the cause of rotary polarization)," Comptes rendus de l'Académie des sciences (Paris), 26 : 535–538.
- ↑ L. Pasteur (1848) "Sur les relations qui peuvent exister entre la forme cristalline, la composition chimique et le sens de la polarisation rotatoire" (On the relations that can exist between crystalline form, and chemical composition, and the sense of rotary polarization), Annales de Chimie et de Physique, 3rd series, 24 : 442–459.
- ↑ Pasteur, Louis (1850) "Recherches sur les propriétés spécifiques des deux acides qui composent l'acide racémique" (Investigations into the specific properties of the two acids that compose racemic acid), Annales de Chimie et de Physique, 3rd series, 28 (3) : 56–99. See also Plate II. (See also the report of the commission that was appointed to verify Pasteur's findings, pp. 99–117.) [in French]
- ↑ George B. Kauffman and Robin D. Myers (1998). "Pasteur's resolution of racemic acid: A sesquicentennial retrospect and a new translation" (PDF). The Chemical Educator. 3 (6): 1–4. doi:10.1007/s00897980257a. Archived from the original (PDF) on 2006-01-17.
- ↑ H. D. Flack (2009). "Louis Pasteur's discovery of molecular chirality and spontaneous resolution in 1848, together with a complete review of his crystallographic and chemical work" (PDF). Acta Crystallographica A. 65 (5): 371–389. doi:10.1107/S0108767309024088. PMID 19687573. Archived from the original (PDF) on 2012-09-06.
- ↑ "J. M. McBride's Yale lecture on history of stereochemistry of tartaric acid, the D/L and R/S systems". Archived from the original on 2014-11-29. Retrieved 2020-03-25.
- ↑ various (2007-07-23). Organic Chemistry. Global Media. p. 65. ISBN 978-81-89940-76-8. Retrieved 2010-06-05.[permanent dead link]
- ↑ "(WO/2008/022994) Use of azabicyclo hexane derivatives".[permanent dead link]
- ↑ J.-M. Kassaian "Tartaric acid" in Ullmann's Encyclopedia of Industrial Chemistry; VCH: Weinheim, Germany, 2002, 35, 671-678. doi:10.1002/14356007.a26_163
- ↑ Blair, G. T.; DeFraties, J. J. (2000). "Hydroxy Dicarboxylic Acids". Kirk Othmer Encyclopedia of Chemical Technology. pp. 1–19. doi:10.1002/0471238961.0825041802120109.a01.
- ↑ Zalkin, Allan; Templeton, David H.; Ueki, Tatzuo (1973). "Crystal structure of l-tris(1,10-phenathroline)iron(II) bis(antimony(III) d-tartrate) octahydrate". Inorganic Chemistry. 12 (7): 1641–1646. doi:10.1021/ic50125a033.
- ↑ Haq, I; Khan, C (1982). "Hazards of a traditional eye-cosmetic--SURMA". JPMA. the Journal of the Pakistan Medical Association. 32 (1): 7–8. PMID 6804665.
- ↑ McCallum, RI (1977). "President's address. Observations upon antimony". Proceedings of the Royal Society of Medicine. 70 (11): 756–63. PMC 1543508. PMID 341167.
- ↑ Alfred Swaine Taylor, Edward Hartshorne (1861). Medical jurisprudence. Blanchard and Lea. p. 61.
- ↑ Joseph A. Maga, Anthony T. Tu (1995). Food additive toxicology. CRC Press. pp. 137–138. ISBN 0-8247-9245-9.
- ↑ Duarte, A.M.; Caixeirinho, D.; Miguel, M.G.; Sustelo, V.; Nunes, C.; Fernandes, M.M.; Marreiros, A. (2012). "ORGANIC ACIDS CONCENTRATION IN CITRUS JUICE FROM CONVENTIONAL VERSUS ORGANIC FARMING". Acta Horticulturae (933): 601–606. doi:10.17660/actahortic.2012.933.78. ISSN 0567-7572. Archived from the original on 2018-06-02. Retrieved 2020-03-25.
- ↑ Blair, G. T.; DeFraties, J. J. (2000). "Hydroxy Dicarboxylic Acids". Kirk Othmer Encyclopedia of Chemical Technology. pp. 1–19. doi:10.1002/0471238961.0825041802120109.a01.
బాహ్య లంకెలు
మార్చు- PDB file for MSE Archived 2018-09-20 at the Wayback Machine